
(14分)Na2S2O3可做分析试剂。它易溶于水,遇酸易分解。某研究小组进行如下实验:
【实验一】Na2S2O3·5H2O的制备
I 实验原理:Na2SO3(aq)+S(s)△ Na2S2O3(aq)
II 实验装置:如图1所示,有关物质的溶解度曲线如图2所示:
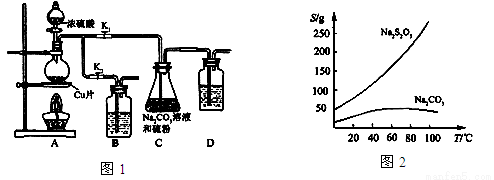
III 实验步骤:
(1)检查装置气密性,按图1所示加入试剂,其中装置B和D中加的是 ,装置C中的硫粉应事先研细并用乙醇润湿,否则会影响 。
(2)打开K1、关闭K2,向圆底烧瓶中加入足量浓硫酸并加热,烧瓶内发生反应的化学方程式: 。C中混合液被气流搅动,反应一段时间后,硫粉的量逐渐减少。
(3)当C中溶液的pH接近7时,打开K2、关闭K1并停止加热。采取该措施的理由是 。
(4)将C中的混合液过滤,将滤液经过 、 、过滤、洗涤、烘干,可得粗产品Na2S2O3·5H2O。
IV 产品检测:
(5)粗产品中可能含有Na2SO3、Na2SO4等杂质,利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论: 。
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液
【实验二】自来水中余氯的测定
含氯消毒剂给自来水消毒后有余氯。测定自来水中余氯含量的方案如下:在250ml碘量瓶中(或具塞锥形瓶中)放置0.5g碘化钾,加10ml稀硫酸,准确量取流动水样100ml(打开自来水龙头,待水流数十秒后再取水样)置于碘量瓶,迅速塞上塞摇动,见水样呈淡黄色,加1ml淀粉溶液变蓝,则说明水样中有余氯。再以C mol/L标准Na2S2O3溶液滴定,至溶液蓝色消失呈无色透明溶液,记下硫代硫酸钠溶液的体积。
(已知:滴定时反应的化学方程式为I2+2Na2S2O3=2NaI+Na2S4O6)
(6)若该自来水是以漂白粉消毒,能说明水样中有余氯的反应离子方程式为 。
(7)按上述方案实验,消耗标准Na2S2O3溶液V mL,该次实验测得自来水样品中余氯量(以游离Cl2计算)为____ mg·L-1。在上述实验过程中,若“塞上塞摇动”动作不够迅速,则测得结果 (填“偏高”“偏低”或“不变”)。
科目:高中化学 来源:2014-2015四川省达州市高一3月月考化学试卷(解析版) 题型:填空题
(2013·华中师大一附中月考)下表是元素周期表主族元素的一部分,短周期元素X的最高正化合价是+5,Y的单质可在空气中燃烧。
W | X | Y |
Z |
请回答下列问题:
(1)Z的元素符号是 ,写出Z的原子结构示意图: 。
(2)W的最高价氧化物不溶于水,但能溶于烧碱溶液,该反应的离子方程式为 。
(3)探究同主族元素性质的一些共同规律,是学习化学的一项重要内容。在下表中列出对H2ZO3化学性质的推测,举例并写出相应的化学方程式(化学方程式中Z用元素符号表示)
编号 | 性质推测 | 化学方程式 |
示例 | 氧化性 | H2ZO3+4HI=Z↓+2I2+3H2O |
1 | ||
2 |
(4)由C、O和Y三种元素组成的化合物OCY中,所有原子的最外层都满足8电子结构。写出该化合物的电子式: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省安庆市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
为实现实验目的,其他主要仪器,所用试剂合理且需要在某个部位放置温度计的是
选项 | 实验目的 | 玻璃实验仪器 | 实验试剂 | 温度计位置 |
A | 制取乙烯 | 圆底烧瓶、集气瓶、带胶塞导气管、酒精灯 | 浓硫酸、乙醇 | 反应液中 |
B | 提纯乙醇 | 蒸馏烧瓶、冷凝管、锥形瓶、承接管 | 含杂质乙醇 | 支气管口 |
C | 中和热测定 | 烧杯、环形玻璃搅拌器 | 氢氧化钠、醋酸 | 酸、碱及反应液中 |
D | 制镜 | 烧杯、试管、酒精灯 | 银氨溶液、葡萄糖 | 水浴的烧杯水中 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁朝阳市三校协作体高三下学期第一次联考理综化学试卷(解析版) 题型:填空题
(15分)化合物AX3和单质X2在一定条件下反应可生成化合物AX5,该反应不能彻底。回答下列问题:
(1)已知AX3的熔点和沸点分别为-93.6 ℃和76 ℃,AX5的熔点为167 ℃。室温时AX3与气体X2反应生成lmol AX5时,放出热量123.8 kJ。该反应的热化学方程式为 。
(2)一定条件下,反应AX3(g)+X2(g) AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行a、b、c三组实验,反应体系总压强随时间的变化如图所示。
AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行a、b、c三组实验,反应体系总压强随时间的变化如图所示。

①用P0表示开始时总压强,P表示平衡时总压强,用α表示AX3的平衡转化率,则α的表达式为 。由此计算实验c中 AX3的平衡转化率:αc为 。若在实验a中再加入0.1mol AX5,再次达平衡后AX3的平衡转化率将 。(填“增大、减小或不变”)
②下列不能说明反应达到平衡状态的是 。
A.混合气体的平均相对分子质量保持不变
B.混合气体密度保持不变
C.体系中X2的体积分数保持不变
D.每消耗1 mol AX3的同时消耗1 mol AX5
③计算实验a从反应开始至到达平衡v(AX5)化学反应速率为 mol/(L·min)。(保留2位有效数字)
④图中3组实验从反应开始至到达平衡时的化学反应速率v(AX5)由大到小的次序为 (填实验序号);与实验a相比,其他两组改变的实验条件是:b 、c 。该反应在实验a和实验c中的化学平衡常数的大小关系是Ka Kc(填“>、< 或 =”),其中Kc= (注意标明单位,且保留小数点后1位)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁朝阳市三校协作体高三下学期第一次联考理综化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.向KI与稀硫酸的混合溶液中通入氧气:4H++O2+6I- = 3I2+2H2O
B.亚硫酸钠溶液与双氧水混合:SO32-+2H2O2 = SO42-+2H2O+O2↑
C.a mol FeI2溶液中通入2a mol Cl2:2Fe2++4I-+3Cl2 = 2I2+2Fe3++6C1-
D.硅酸钠溶液中通入过量的CO2:SiO32-+CO2+H2O = H2SiO3↓+CO32-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省高三4月联考理综化学试卷(解析版) 题型:选择题
金属锂燃料电池是一种新型电池,比锂离子电池具有更高的能量密度。它无电时也无需充电,只需更换其中的某些材料即可,其工作示意图如下,下列说法正确的是
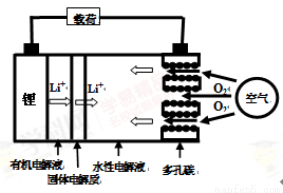
A.放电时,空气极为负极
B.放电时,电池反应为:4Li+O2=2Li2O
C.有机电解液可以是乙醇等无水有机物
D.在更换锂电极的同时,要更换水性电解液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年贵州省八校联盟高三第二次联考理综化学试卷(解析版) 题型:填空题
选考(15)化学与技术
侯氏制碱法的生产流程可表示如下,请回答下列问题:
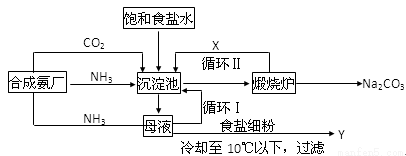
(1)沉淀池中加入(或通入)有关物质的顺序为_____________→___________→___________
(2)写出上述流程中X、Y的化学式:X____________Y___________
(3)写出沉淀池中发生的化学反应方程式__________________________________________
(4)侯氏制碱法的生产流程中可以循环使用的物质主要为____________、______________
(5)从沉淀池中取出沉淀的操作是___________,为了进一步提纯NaHCO3晶体,可采用_______法
(6)若在煅烧炉中燃烧的时间较短,NaHCO3将化解不完全。现若取10.5g NaHCO3固体,加热一定时间后,剩余固体的质量为7.1g,如果把此剩余固体全部加入到200mL 1mol/L的盐酸中,充分反应后溶液中H+的物质的量浓度为___________mol/L(溶液体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市朝阳区高三4月第一次综合练习理综化学试卷(解析版) 题型:选择题
如图为锌铜显示原电池装置图,下列说法不正确
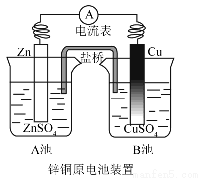
A.电子由Zn极流向Cu极
B.该装置的总反应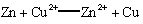
C.一段时间后,A池带正电荷,B池带负电荷
D.取出盐桥,电流计指针不再偏转
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com