
| A. | 含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mo1•L-1 | |
| B. | 标准状况下,22.4L水所含的分子数为NA | |
| C. | 常温常压下NO2和N2O4混合气体22.4L,其中含有的原子总数为0.3NA | |
| D. | 常温下,4gCH4含有NA个C-H共价键 |
分析 A、含NA个Na+的Na2O溶解于1L水中,溶液体积大于1L;
B、标况下,水为液态;
C、常温常压下,气体摩尔体积大于22.4L/mol;
D、求出甲烷的物质的量,然后根据1mol甲烷中含4molC-H键来分析.
解答 解:A、含NA个Na+的Na2O溶解于1L水中,溶液体积大于1L,故Na+的物质的量浓度小于1mo1•L-1,故A错误;
B、标况下,水为液态,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、常温常压下,气体摩尔体积不是22.4L/mol,故22.4L混合气体的物质的量不能计算,则含有的原子总数不能计算,故C错误;
D、4g甲烷的物质的量为0.25mol,而1mol甲烷中含4molC-H键,故0.25mol甲烷中含1molC-H键即NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃1L的0.1mol•L-1H2SO4溶液 | |
| B. | T℃1L 0.2mol•L-1H2SO4溶液中加入1L 0.2mol•L-1NaOH溶液后得到的2L溶液 | |
| C. | 25℃a mol•L-1NaHSO4溶液[已知50ml amol•L-1Ba(OH)2溶液与100mL amol•L-1NaHSO4溶液混合后pH=7] | |
| D. | T℃c(OH-)=10-13mol•L-1的某盐溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氧化亚铜(Cu2O)作为一种重要的无机化工原料,在涂料、有色玻璃和催化剂等领域有着广泛的用途.回答下列问题:
氧化亚铜(Cu2O)作为一种重要的无机化工原料,在涂料、有色玻璃和催化剂等领域有着广泛的用途.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 是环戊烯的结构简式,可进一步简写为
是环戊烯的结构简式,可进一步简写为 ,环戊烯的化学性质跟链烯烃相似.
,环戊烯的化学性质跟链烯烃相似.
 )臭氧化分解各种产物的结构简式及其物质的量之比n(HCHO):n(CH3COCHO)=2:1.
)臭氧化分解各种产物的结构简式及其物质的量之比n(HCHO):n(CH3COCHO)=2:1.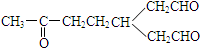 ,A经催化加氢得产物B,B的分子式是C10H20.分析数据表明,分子B内含有六元碳环.则A的键线式为
,A经催化加氢得产物B,B的分子式是C10H20.分析数据表明,分子B内含有六元碳环.则A的键线式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1 817 | 2 745 | 11 578 |
| Y | 738 | 1 451 | 7 733 | 10 540 |
| Z | 496 | 4 562 | 6 912 | 9 543 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 甲烷的燃烧热为890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3KJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 已知在120℃,101kPa下,1gH2燃烧生成水蒸气放出121kJ热量,其热化学方程式为H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242kJ•mol-1 | |
| D. | 25℃,101Kpa时,强酸与强碱的稀溶液发生反应的中和热为57.3kJ•mol-1,硫酸稀溶液与氢氧化钾稀溶液反应的热化学方程式可表示为:H2SO4(aq)+2KOH(aq)═K2SO4(aq)+2H2O(1)△H=-114.6kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在25mL 0.1mol?L-1 NaOH溶液中逐滴加入0.2mol?L-1 CH3COOH溶液,曲线如图所示,下列判断正确的是( )
在25mL 0.1mol?L-1 NaOH溶液中逐滴加入0.2mol?L-1 CH3COOH溶液,曲线如图所示,下列判断正确的是( )| A. | B点,a=12.5 | |
| B. | D点,c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| C. | 在A、B间存在一点,此点水的电离程度最大 | |
| D. | 在C点升温,CH3COOH电离程度增大,CH3COO-的水解程度减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com