
为了证明一水合氨(NH3·H2O)是弱电解质,甲、乙、丙三人分别选用下列试剂进行实验:0.010 mol·L-1氨水、0.1 mol·L-1NH4Cl溶液、NH4Cl晶体、酚酞试剂、pH试纸、蒸馏水。
(1)甲用pH试纸测出0.010 mol·L-1氨水的pH为10,则认定一水合氨是弱电解质,你认为这一方法是否正确?________(填“是”或“否”)并说明理由_______________________
________________________________________________________________________。
(2)乙取出10 mL 0.010 mol·L-1氨水,用pH试纸测出其pH=a,然后用蒸馏水稀释至1 000 mL,再用pH试纸测出其pH为b,若要确认NH3·H2O是弱电解质,则a、b值应满足什么关系?________(用“等式”或“不等式”表示)。
(3)丙取出10 mL 0.010 mol·L-1氨水,滴入2滴酚酞溶液,显粉红色,再加入NH4Cl晶体少量,颜色变浅。你认为这一方法能否证明NH3·H2O是弱电解质?并说明原因:
________________________________________________________________________
________________________________________________________________________。
(4)请你根据所提供的试剂,再提出一个合理又简便的方案证明 NH3·H2O是弱电解质:
NH3·H2O是弱电解质:
________________________________________________________________________
________________________________________________________________________。
解析:(1)因为一水合氨若是强电解质,则0.010 mol·L-1氨水溶液中c(OH-)应为0.010 mol·L-1,pH=12,事实上0.010 mol·L-1氨水的pH仅为10,故可判断一水合氨是弱电解质。
(2)弱碱溶液每稀释10倍,溶液pH减小不足一个单位,故当用蒸馏水稀释100倍时,其pH=b>a-2,但小于a。
(3)因少量晶体的加入对溶液体积的影响可以忽略不计,故溶液颜色变浅只能是由于平衡移动使溶液中OH-浓度减小导致的,故由此现象可以判断一水合氨是弱电解质。
(4)如果NH3·H2O是弱电解质,则它的强酸盐水解显酸性,可利用这一原理设计实验证明NH3·H2O是弱电解质。
答案:(1)是 若是强电解质,则0.010 mol·L-1氨水溶液中c(OH-)应为0.010 mol·L-1,pH=12
(2)a-2<b<a
(3)能,因为0.010 mol·L-1氨水(滴有酚酞)中加入氯化铵晶体后颜色变浅,有两种可能:一是氯化铵在水溶液中水解显酸性,加入氨水中使溶液的pH降低;二是NH 使NH3·H2O的电离平衡(NH3·H2ONH
使NH3·H2O的电离平衡(NH3·H2ONH +OH-)逆向移动,从而使溶液的pH降低。这两种可能都证明NH3·H2O是弱电解质
+OH-)逆向移动,从而使溶液的pH降低。这两种可能都证明NH3·H2O是弱电解质
(4)取一张pH试纸,再用玻璃棒蘸取0.1 mol·L-1NH4Cl溶液,滴在pH试纸上,显色后跟标准比色卡比较测出pH,pH>7(方案合理即可)。


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
过氧乙酸是在抗SARS病毒期间常使用的一种高效杀毒剂,其分子式为C2H4O3,它具有氧化性,漂白作用,下列物质中漂白作用原理与过氧乙酸不同的是( )
A.氯水(次氯酸) B.臭氧 C.活性炭 D.过氧化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应①:CO(g)+CuO(s)CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A.反应①的平衡常数K1=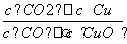
B.反应③的平衡常数K=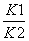
C.对于反应③,恒容时,温度升高,H2浓度减小,则该反应的焓变为正值
D.对于反应③,恒温恒容下,增大压强,H2浓度一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)用化学方程式表示SO2形成硫酸型酸雨的反应:___________________________
________________________________________________________________________。
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是_________________________________________________________________
________________________________________________________________________。
(3)吸收液吸收SO2的过程中,pH随n(SO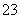 )∶n(HSO
)∶n(HSO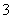 )变化关系如下表:
)变化关系如下表:
| n(SO | 91∶9 | 1∶1 | 9∶91 |
| pH | 8.2 | 7.2 | 6.2 |
①由上表判断,NaHSO3溶液显________性,用化学平衡原理解释:_____________。
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):________。
a.c(Na+)=2c(SO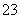 )+c(HSO
)+c(HSO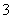 )
)
b.c(Na+)>c(HSO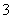 )>c(SO
)>c(SO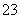 )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(SO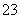 )+c(HSO
)+c(HSO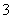 )+c(OH-)
)+c(OH-)
(4)(201 2·福建高考节选)能证明Na2SO3溶液中存在SO
2·福建高考节选)能证明Na2SO3溶液中存在SO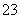 +H2OHSO
+H2OHSO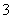 +OH-水解平衡的事实是________(填序号)。
+OH-水解平衡的事实是________(填序号)。
A.滴入酚酞溶液变红 ,再加入H2SO4溶液后红色褪去
,再加入H2SO4溶液后红色褪去
B.滴入酚酞溶液变红,再加入氯水后红色褪去
C.滴入酚酞溶液变红,再加入BaCl2溶液后产生沉淀且红色褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于常温下电解质溶液的叙述中,正确的是( )
A.碳酸氢铵溶液和足量氢氧化钠溶液混合的离子反应:HCO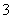 +OH-===CO
+OH-===CO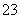 +H2O
+H2O
B.等物质的量浓度、等体积的氨水和盐酸混合后,c(H+)+c(NH )=c(Cl-)+c(OH-)
)=c(Cl-)+c(OH-)
C.等物质的量浓度的NH4Cl溶液和NH3·H2O溶液,溶液中c(NH )前者大于后者
)前者大于后者
D.25℃时,pH=8的0.1 mol·L-1NaX溶液中由水电离出的c(OH-)=1×10-8 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物在氧气中充分燃烧,生成的水蒸气和二氧化碳的物质的量之比为1∶1,由此可以得出的结论是
( )
A.该有机物中C、H、O的原子个数比为1∶2∶3
B.分子中C、H的原子个数比为1∶2
C.有机物中必定含氧
D.有机物中必定不含氧
查看答案和解析>>
科目:高中化学 来源: 题型:
核磁共振氢谱是指有机物分子中的氢原子核所处的化学环境(即其附近的基团)不同,表现出的核磁性就不同,代表核磁性特征的峰在核磁共振图中坐标的位置(化学位移,符号为δ)也就不同。现有一物质的核磁共振氢谱如下图所示。则可能是下列物质中的
( )
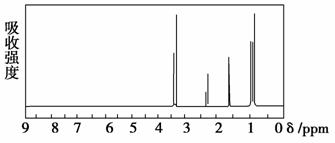
A.CH3CH2CH3 B.CH3CH2CH2OH
C.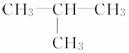 D.CH3CH2CHO
D.CH3CH2CHO
查看答案和解析>>
科目:高中化学 来源: 题型:
将某溶液逐滴加入到氢氧化铁胶体中,开始产生沉淀,后又溶解的是( )
A.2 mol·L-1的氢氧化钠溶液 B.2 mol·L-1的硫酸溶液
C.2 mol·L-1的硫酸镁溶液 D.2 mol·L-1的乙醇溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质性质的说法不合理的是
A.金属Mg与稀硫酸和CO2均能反应,其反应类型相同
B.FeCl3、Na2O2、Cu2S均可由相应单质直接化合生成
C.SO2气体通入紫色石蕊试液中,溶液先变红后褪色
D.氢氧化铝、碳酸铵、碳酸氢钠、甘氨酸都既能与盐酸反应,又能与氢氧化钠溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com