
| A. | 2 个 | B. | 3 个 | C. | 4 个 | D. | 5 个 |
分析 ①混合物是由多种物质组成的物质,化合物是由不同种元素组成的纯净物;
②混合物是由多种物质组成的物质,化合物是由不同种元素组成的纯净物;
③水溶液中或熔融状态下完全电离的电解质为强电解质;
④结构相似、组成上相差CH2的有机物互为同系物;
⑤分散质微粒直径1-100nm相差的分散系为胶体,分散质微粒直径小于1nm形成的分散系为溶液,大于100nm形成的分散系为浊液;
⑥质子数相同中子数不同的同种元素的不同原子为同位素;
解答 解:①HDO、双氧水、干冰、碘化银都是一种物质组成的纯净物,不同元素组成均为化合物,故①正确;
②淀粉是高分子化合物、盐酸是氯化氢水溶液、水玻璃为硅酸钠水溶液、氨水是氨气的水溶液均为混合物,故②错误;
③明矾为硫酸铝钾、小苏打为碳酸氢钠、硫酸钡为盐、生石灰为氧化钙,熔融状态下完全电离均为强电解质,故③正确;
④甲醇、乙二醇、甘油分子中所含羟基官能团个数不同,不属于同系物,故④错误;
⑤牛奶、豆浆、淀粉液均为胶体,碘酒是碘单质的水溶液不是胶体,故⑤错误;
⑥H2、D2、T2是氢气单质,不是原子,不能互为同位素,故⑥错误;
故选A.
点评 本题考查物质的分类知识,熟记各类物质的概念是解决该题的关键,题目难度不大.


 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:选择题
| 类别 选项 | 纯净物 | 混合物 | 电解质 | 非电解质 |
| A | 生理盐水 | 纯碱 | 液态硝酸钾 | 蔗糖 |
| B | 氧化钙 | 海水 | 铜 | 乙醇 |
| C | 胆矾 | 氢氧化铁胶体 | 氯化银 | 二氧化碳 |
| D | 氢氧化钠 | 空气 | 硫酸钠溶液 | 食醋 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 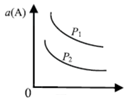 图:p1>p2,则此反应只能在高温下自发进行 | |
| B. |  图:此反应的△H<0,且T1<T2 | |
| C. |  图:表示t1时刻一定是使用催化剂对反应速率的影响 | |
| D. |  图:表示t1时刻增大B的浓度对反应速率的影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{4}{5}$ v(NH3)=v(O2) | B. | $\frac{4}{5}$ v(O2)=v(NO) | C. | $\frac{5}{6}$ v(O2)=v(H2O) | D. | $\frac{2}{3}$ v(NH3)=v(H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,2g H2中含有的氢原子数为2NA | |
| B. | 标准状况下,22.4L水中含有的分子数为NA | |
| C. | 1L 0.1mol/L NaCO3溶液中含有的钠离子数为NA | |
| D. | 将1mol Cl2通入足量FeCl2溶液中充分反应,转移电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3(m-n) | B. | m+$\frac{n}{3}$ | C. | $\frac{n-m}{3}$ | D. | $\frac{4n-m}{12}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com