
【题目】在100℃时,将0.40mol NO2气体充入2L的密闭容器中,发生如下反应:2NO2(g)N2O4(g)△H<0.监测反应获得如表数据:下列说法正确的是( )
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
A.0~20 s内,v(NO2)=0.005 mol?L﹣1?s﹣1
B.59 s时,c(NO2)一定大于0.12 mol?L﹣1
C.若仅将起始时充入NO2的量增至0.80 mol,则该反应的平衡常数K> ![]()
D.若上述反应在120℃时进行,则反应至80 s时,n(N2O4)<0.08 mol
【答案】D
【解析】解:A、0~20 s内,v(N2O4)= ![]() =0.00125 molL﹣1s﹣1 , 根据速率之比等于对应物质的化学计量数之比,所以v(NO2)=0.0025 molL﹣1s﹣1 , 故A错误;
=0.00125 molL﹣1s﹣1 , 根据速率之比等于对应物质的化学计量数之比,所以v(NO2)=0.0025 molL﹣1s﹣1 , 故A错误;
B、60 s时△n(N2O4)=0.08mol,所以60s时△n(NO2)=0.16mol,所以如果59 s未平衡,n(NO2)>0.40﹣0.16=0.24mol,则c(NO2)一定大于0.12 molL﹣1 , 如果平衡c(NO2)等于0.12 molL﹣1 , 故B错误;
C、60s反应达平衡状态,平衡常数为:K=  =
= ![]() ,所以若仅将起始时充入NO2的量增至0.80 mol,则该反应的平衡常数K=
,所以若仅将起始时充入NO2的量增至0.80 mol,则该反应的平衡常数K= ![]() ,故C错误;
,故C错误;
D、2NO2(g)N2O4(g)△H<0,正反应是放热反应,升高温度平衡向逆反应方向移动,所以反应在120℃时进行,则反应至80 s时,n(N2O4)<0.08 mol,故D正确;
故选D.
【考点精析】通过灵活运用化学平衡状态本质及特征,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)即可以解答此题.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.NO2与水的反应:3NO2+H2O═2NO3﹣+NO+2H+
B.氯气通入水中:Cl2+H2O═2H++Cl﹣+ClO﹣
C.向NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH﹣ ![]() NH3↑+H2O
NH3↑+H2O
D.向硅酸钠溶液中通入SO2:SiO32﹣+2H+═H2SiO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20.其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1 . B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半.请回答下列问题:
(1)A是 , B是 , E是 .
(2)写出C元素基态原子的电子排布式 .
(3)用轨道表示式表示D元素原子的价电子构型 .
(4)元素B与D的电负性的大小关系是 , C与E的第一电离能的大小关系是 . (填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( ) 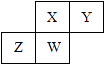
A.原子半径:W>Z>Y>X
B.最高价氧化物对应水化物的酸性:X>W>Z
C.最简单气态氢化物的热稳定性:Y>X>W>Z
D.元素X、Z、W的最高化合价分别与其主族序数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生为了探究钠与CO2的反应,利用如图装置进行实验.(已知PdCl2能被CO还原得到黑色的Pd)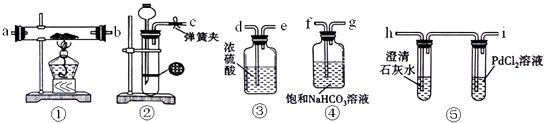
(1)请将上图各装置连接完整(填写装置中序号)→→→→ .
(2)若用稀盐酸与CaCO3反应制备CO2 , 在加稀盐酸时,发现CaCO3与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向装置②长颈漏斗中加入的试剂是 .
A.CCl4
B.H2SO4溶液
C.硝酸钠溶液
D.植物油
(3)检查装置②的气密性,方法是 . 装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让CO2充满整个装置,当观察到时再点燃酒精灯.装置④的作用 .
(4)通入CO2的量不同可能会导致生成的产物不同.假如反应过程中有下列两种情况,按要求分别写出两种情况时的化学方程式.I.当装置⑤PdCl2溶液中观察到有黑色沉淀产生,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体,写出此情况时钠与CO2反应的化学方程式 .
II.当装置①中钠的质量为0.23g时,充分反应后,将装置①中的固体加入到足量稀盐酸中,产生112mL的CO2气体(标况下测定),装置⑤PdCl2溶液中没有观察到黑色沉淀产生,写出此情况时钠与CO2反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式正确的是( )
A.用氯化钠溶液做导电实验,灯泡发光:NaCl ![]() Na++Cl﹣
Na++Cl﹣
B.氢氧化铁沉淀溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O
C.石灰水表面漂着的“白膜”可用醋酸溶解:CaCO3+2H+═Ca2++H2O+CO2↑
D.向硫酸氢钠溶液中滴加氢氧化钡溶液至刚好为中性:2H++SO42﹣+Ba2++2OH﹣═BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( ) 
A.常压下五种元素的单质中,Z单质的沸点最高
B.Y,Z的阴离子电子层结构都与R原子的相同
C.W的氢化物的稳定性比X的氢化物的稳定性高
D.Y元素的非金属性比W元素的非金属性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 钠、铁和铜一样都能在氯气中燃烧生成金属氯化物。
B. 液氯是氯气的水溶液,它能使干燥的有色布条褪色。
C. 氯气跟变价金属反应生成高价金属氯化物。
D. 氯水具有杀菌、漂白作用是因为氯水中含有强氧化性的次氯酸。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com