某饱和一元醇30g与足量金属钠反应,共收集到标况下气体5.6L.(假设气体无损失)
(1)则此醇的分子式为______
(2)写出此醇可能的结构简式:______.
【答案】
分析:醇和钠反应,生成氢气,实际反应的方程式是2ROH+2Na=2RONa+H
2,5.6L氢气是0.25摩尔,根据方程式可求出醇的物质的量,再求出醇的分子量,那么确定该醇就是丙醇,正丙醇或异丙醇,然后确定醇的分子式和结构简式.
解答:解:(1)醇和钠反应,生成氢气,实际反应的方程式是2ROH+2Na=2RONa+H
2,5.6L氢气是0.25摩尔,根据方程式:醇的物质的量就是0.25×2=0.5mol,醇的相对分子质量:M=
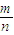
=
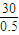
=60,那么该醇就是丙醇,此醇的分子式为 C
3H
8O,故答案为:C
3H
8O;
(2)丙醇可能的结构简式:CH
3CH
2CH
2OH或CH
3CH(OH)CH
3,故答案为:CH
3CH
2CH
2OH或CH
3CH(OH)CH
3;
点评:本题考查化学方程式的有关计算,难度不大,注意掌握方程式的计算是解题的关键.

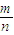 =
=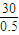 =60,那么该醇就是丙醇,此醇的分子式为 C3H8O,故答案为:C3H8O;
=60,那么该醇就是丙醇,此醇的分子式为 C3H8O,故答案为:C3H8O;
