
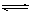 mD(g)+E(g),经过5min后达到化学平衡,此时测得D为0.2 mol。又知5min内用E表示的平均反应速
mD(g)+E(g),经过5min后达到化学平衡,此时测得D为0.2 mol。又知5min内用E表示的平均反应速 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源:不详 题型:计算题
| 实验 编号 | T/K | 大理石 规格 | HNO3浓度 /(mol/L) | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (I)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和③探究________________对该反应速率的影响; (Ⅲ)实验①和④探究________________对该反应速率的影响。 |
| ② | 298 | 粗颗粒 | 1.00 | |
| ③ | 298 | 细颗粒 | 2.00 | |
| ④ | 308K | 粗颗粒 | 2.00 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2C(g)+3D(g),取1 mol A和2 mol B置于2L容器内。1分钟后,测得容器内A的浓度为0.2 mol/L。
2C(g)+3D(g),取1 mol A和2 mol B置于2L容器内。1分钟后,测得容器内A的浓度为0.2 mol/L。
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 2 SO3反应。5分钟后反应达到化学平衡状态,测得容器中气体压强变为原来的90%。求
2 SO3反应。5分钟后反应达到化学平衡状态,测得容器中气体压强变为原来的90%。求查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g), 若经2s后测得C的浓度为0.6 mo1·L-1,现有下列几种说法:
2C(g), 若经2s后测得C的浓度为0.6 mo1·L-1,现有下列几种说法:| A.①③ | B.①④ | C.②③ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①>②>③ | B.②>①>③ | C.③>①>②. | D.②>③>① |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.开始时的反应速率:V(锌粒)>V(锌粉) |
| B.溶液温度升高的快慢:T(锌粒)>T(锌粉) |
| C.最后放出H2的总量:n(锌粒)>n(锌粉) |
| D.达平衡时正逆反应的速率相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.反应速率用于衡量化学反应的快慢 |
| B.决定反应速率的主要因素是反应物的性质 |
| C.可逆反应达到化学平衡时,正、逆反应速率都为0 |
| D.增大反应物浓度,提高反应物温度都能增大反应速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com