
(14分) (1)键线式 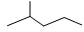 表示的分子式 _____;名称是 。
表示的分子式 _____;名称是 。
(2) 中含有的官能团的名称为 。
中含有的官能团的名称为 。
(3)写出符合分子式为C5H12的所有同分异构体的结构简式以及它们的习惯命名:
________________________________________________________________________________________
(4)含有杂质的工业乙醇的蒸馏装置中,玻璃仪器有酒精灯、蒸馏瓶、_________、_________、尾接管、锥形瓶。
科目:高中化学 来源:2010—2011学年山东省德州一中高一下学期期中考试化学试卷 题型:填空题
(14分)已知A、B、C、D、E是短周期的5种元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零;C、D、E三种元素的最高价氧化物对应水化物之间可以两两反应;A与C同主族;B与E同主族;E的单质为黄色晶体,易溶于二硫化碳。
(1)请写出B、D元素的名称:B ,D 。
(2)画出C元素的离子结构示意图 。
(3)写出D的单质与C的最高价氧化物对应水化物之间反应的离子方程式
(4)A、B、C三种元素形成的化合物为 , 所含的化 学键类型为 。
学键类型为 。
(5)B、C、D三种元素的离子半径由大到小的排列顺序为 (用离子符号表示)。
查看答案和解析>>
科目:高中化学 来源:2011届重庆市七区2011届高三第一次调研测试(理综)化学试卷 题型:填空题
(14分)
现有A、B、C、D、E、F六种短周期元素,A、E处于同一主族且E是短周期元素中原子半径最大的元素(不含稀有气体)。已知C的原子序数等于A、B的原子序数之和,D的原子序数等于A、C的原子序数之和。人类已知的化合物中,有一类化合物的种类已超过三千万,这类化合物中一般都含有A、B两种元素。F是一种生活中常用的金属。根据以上信息,回答下列问题:
(1)元素B在周期表中的位置是 。
(2)F的 单质与E的最高价氧化物对应水化物反应的化学方程式是 。
单质与E的最高价氧化物对应水化物反应的化学方程式是 。
(3)C、D最低价氢化物稳定性的强弱顺序是 (填化学式) ;D、E、F原子半径的大小顺序是 (填元素符号)。
(4)在A、C、D组成的化合物中,既有离子键又有共价键的是 (填化学式)。
(5)在A、B、D中,由两种或三种元素组成两种可以反应的阴离子,该反应的离子方程式是 。
(6)化合物BA4D与O2、稀硫酸可组成燃 料电池,此电池的负极反应式是 。
料电池,此电池的负极反应式是 。
查看答案和解析>>
科目:高中化学 来源:2012届四川省成都市高三第二次诊断性检测理综试卷(带解析) 题型:填空题
(14分)巳知 元索,
元索,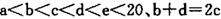 。A2为常温常压下密度最小的气体,B的单质有多种同素异形体,其中一种为质软灰黑色固体。C的最外层电子数是电子层数的2. 5倍。用E的单质制作的餐具不宜长期存放酸性、碱性或咸味食物。
。A2为常温常压下密度最小的气体,B的单质有多种同素异形体,其中一种为质软灰黑色固体。C的最外层电子数是电子层数的2. 5倍。用E的单质制作的餐具不宜长期存放酸性、碱性或咸味食物。
(1) B的原子结构示意图为_________;E在元素周期表中的位置________。
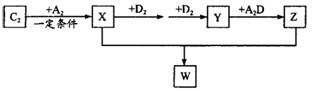
(2) 已知C2及其化合物有以下转化关系(部分物质已省略):
①将已收集满气体Y的试管管口倒扣在水面下,可以观察到的现象是________;其化学反应方程式为________; W的晶体类型为________;将E单质与Z的极稀溶液混合,还原产物只有W,则该反应的离子方程式为________________________。
②上述合成X的反应处于平衡状态时,气体X的浓度为C(X)(如图)。在恒温恒容条件下,t1时刻通人X将X的浓度变为2c(X)。请在下图画出平衡移动过程中X浓度的变化趋势图。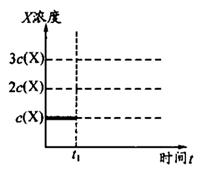
(3) 由其中三种元素形成的只含极性键、具有18电子的共价化合物为________ (写结构简式,至少2种)。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省成都市高三第二次诊断性检测理综试卷(解析版) 题型:填空题
(14分)巳知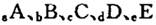 元索,
元索, 。A2为常温常压下密度最小的气体,B的单质有多种同素异形体,其中一种为质软灰黑色固体。C的最外层电子数是电子层数的2. 5倍。用E的单质制作的餐具不宜长期存放酸性、碱性或咸味食物。
。A2为常温常压下密度最小的气体,B的单质有多种同素异形体,其中一种为质软灰黑色固体。C的最外层电子数是电子层数的2. 5倍。用E的单质制作的餐具不宜长期存放酸性、碱性或咸味食物。
(1) B的原子结构示意图为_________;E在元素周期表中的位置________。
(2) 已知C2及其化合物有以下转化关系(部分物质已省略):
①将已收集满气体Y的试管管口倒扣在水面下,可以观察到的现象是________;其化学反应方程式为________; W的晶体类型为________;将E单质与Z的极稀溶液混合,还原产物只有W,则该反应的离子方程式为________________________。
②上述合成X的反应处于平衡状态时,气体X的浓度为C(X)(如图)。在恒温恒容条件下,t1时刻通人X将X的浓度变为2c(X)。请在下图画出平衡移动过程中X浓度的变化趋势图。

(3) 由其中三种元素形成的只含极性键、具有18电子的共价化合物为________ (写结构简式,至少2种)。
查看答案和解析>>
科目:高中化学 来源:2012届吉林省高二下学期第一次月考化学试卷 题型:填空题
(14分)已知A、B、C、D、E都是元素周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。B原子的p轨道半充满,形成的氢化物的沸点是同主族元素的氢化物中最低的。D原子得到一个电子后3p轨道全充满。A+比D原子形成的离子少一个电子层。C与A形成A2C型离子化合物。E的原子序数为26,E原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物。
请根据以上情况,回答下列问题:
(1)含有元素A的盐的焰色反应为 。许多金属盐都可以发生焰色反应,其原因是 。
(2)C的氢化物分子的键角是 ,属于 分子。(填“极性”或“非极性”)
(3)BD3的中心原子的杂化类型是
(4)E的一种常见配合物E(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断E(CO)5的晶体类型为 。
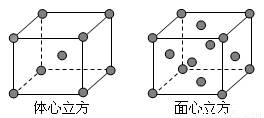
(5)金属E单质的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。体心立方晶胞和面心立方晶胞中实际含有的E原子个数之比为____ ___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com