
实验室制取氯气并回收氯化锰,能达到该实验目的的装置是

A.用装置甲制取氯气 B.用装置丙分离二氧化锰和氯化锰溶液
C.用装置乙吸收制取氯气的尾气 D.用装置丁蒸干氯化锰溶液制 MnCl2·4H2O
科目:高中化学 来源:2014-2015学年天津南开区高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值,下列叙述错误的是
A.在18g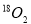 中含有
中含有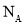 个氧原子
个氧原子
B.在反应KIO3+6HI =KI +3I2+3H2O中,每生成3 mol I2转移的电子数为6 NA
C.常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA
D.25℃,1L pH=13的NaOH溶液中含有OH-的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闸北区高三上学期期末化学试卷(解析版) 题型:选择题
关于三种有机物叙述错误的是(—SH的性质类似于—OH)

A.都能发生酯化反应
B.都能与NaOH反应
C.甲的苯环上的一氯代物有4种
D.丙的分子式为C10H15ON,苯环上的一氯代物有3种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市普陀区高三一模化学试卷(解析版) 题型:填空题
(本题共12分)铜是生命必需的元素,也是人类广泛使用的金属。
28.现代工业上,主要采用高温冶炼黄铜矿(CuFeS2,也可表示为Cu2S?Fe2S3)的方法获得铜。火法炼铜首先要焙烧黄铜矿:2CuFeS2+4O2 Cu2S+3SO2+2FeO,反应中被还原的元素有 ,每转移0.6mol电子,有 mol硫被氧化。产物中的SO2是一种大气污染物,可选用下列试剂中的 吸收(选填编号)。
Cu2S+3SO2+2FeO,反应中被还原的元素有 ,每转移0.6mol电子,有 mol硫被氧化。产物中的SO2是一种大气污染物,可选用下列试剂中的 吸收(选填编号)。
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.CaCl2
29.Cu2O投入足量的某浓度的硝酸中,若所得气体产物为NO和NO2的混合物,且体积比为1﹕1,发生反应的化学方程式为: 。
30.某同学通过电化学原理实现了如下转化:Cu+2H+→Cu2++H2↑,则H2在 极获得(填写电极名称)。
31.向氯化铜和氯化铁的混合溶液中加入氧化铜粉末会产生新的沉淀,写出该沉淀的化学式 。请用平衡移动的原理,结合必要的离子方程式,对此现象作出解释 。
32.将SO2气体通入CuCl2溶液中,生成CuCl沉淀的同时,还有产物 (填写化学式)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市普陀区高三一模化学试卷(解析版) 题型:选择题
关于合成氨反应中平衡常数的讨论,一定正确的是
A.平衡常数越大,则H2转化率越大
B.平衡常数越小,则平衡向逆反应方向移动
C.只改变某一条件使平衡常数增大,则正反应速率增大
D.只改变某一条件使平衡常数减小,则H2转化率减小
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市普陀区高三一模化学试卷(解析版) 题型:选择题
化学反应中,有时“一种物质过量,另一种物质仍不能完全反应”。下列反应中不存在此类情况的是
A.铁片与过量浓硝酸(常温) B.铜粉与过量浓硝酸(常温)
C.浓盐酸与过量MnO2(共热) D.浓硫酸与过量铜片(共热)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市嘉定区高三一模化学试卷(解析版) 题型:计算题
计算题
53.某同学查得Ba(OH)2?8H2O晶体在20℃时的溶解度为3.9 g/100g水,则20℃时,Ba(OH)2饱和溶液的质量分数为______________________ (答案保留2位小数) 。
54.过氧化钡(BaO2)是一种常用的氧化剂。工业上制取过氧化钡的方法之一是2BaO+O2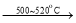
2BaO2。现有16.0吨的氧化钡在足量的氧气中加热反应后,固体的质量变为17.6吨。那么实际参加反应的氧化钡的质量为______________吨。
取不同质量由Ba(OH)2?nH2O和BaCO3组成的样品,加水溶解后加入80 mL 1.0 mol/L的盐酸,并不断地搅拌,所得CO2气体的体积(已换算为标准状况)与加入样品的质量关系通过描点得到下图(在此过程中不考虑Ba(HCO3)2的生成和CO2的溶解)。请计算:
55.在11.58 g样品中BaCO3的质量为多少g?(写出计算过程)
56.化学式Ba(OH)2?nH2O中n的值为多少?(写出计算过程)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市嘉定区高三一模化学试卷(解析版) 题型:选择题
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是
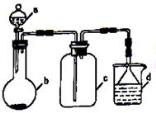
选项 | a中的物质 | b中的物质 | C中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 稀硝酸 | Cu | NO2 | H2O |
C | 稀硫酸 | FeS | H2S | NaOH溶液 |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市长宁区高三上学期教学质量检测化学试卷(解析版) 题型:计算题
(本题共14分)氨在工业生产中有广泛的用途。
54.某工厂平均每天产生约600 m3废氨水(该氨水浓度为153 mg/L,密度为1 g/cm3),该废氨水中氨的物质的量浓度为_____________。
55.若含0.800 mol NH3的某氨水溶液质量为54.0 g,向该溶液通入二氧化碳至反应完全,析出晶体后过滤,得到滤液31.2g,则NH4HCO3的产率为_______%。(保留1位小数)
56.NH3常用于制备NO。4NH3+5O2 →4NO+6H2O;(不考虑NO与氧气的反应),设空气中氧气的体积分数为0.20,氮气体积分数为0.80。为使NH3恰好完全氧化为NO,氨—空气混合物中氨的体积分数为________。
57.硫酸工业的尾气可以使用氨水进行吸收,既防止了有害物质的排放,也同时得到副产品氮肥。已知吸收尾气后的氨水全部转化为铵盐。取两份相同体积的铵盐溶液,一份中加入足量硫酸,产生0.09mol SO2(假设气体已全部逸出,下同);另一份中加入足量Ba(OH)2,产生0.16mol NH3,同时得到21.86g沉淀。通过计算,求铵盐溶液中各溶质成分与物质的量浓度之比。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com