
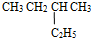 和
和 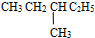 ⑤
⑤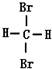 和
和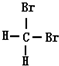
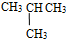 ⑦C2H5OH和C4H9OH
⑦C2H5OH和C4H9OH分析 同素异形体是同种元素组成的性质不同的单质之间的互称;
同位素是质子数相同而中子数不同的同元素的不同原子;
同分异构体是具有相同的分子式和不同结构的有机物之间的互称;
结构、分子式一样的化合物属于同种物质;
结构相似,分子相差一个或多个CH2的有机物为同系物.
解答 解:①O2与O3是由氧元素组成的不同单质,则互为同素异形体;
②12C与14C的质子数都是6,而中子数分别为6、8,且二者都是原子,则互为同位素;
④CH3CH2CH(C2H5)CH3和CH3CH2CH(CH3)C2H5的分子式都为C6H14,结构相同,则为同一化合物;
⑤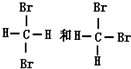 的分子式相同、结构相同,则为同一化合物;
的分子式相同、结构相同,则为同一化合物;
⑥CH3CH2CH2CH3 和(CH3)2CHCH3的分子式都是C4H10,但结构不同,则这两种有机化合物互为同分异构体;
⑦C2H5OH和C4H9OH,结构相似,分子组成相差2个CH2,互为同系物;
故答案为:①;②;⑥;④⑤;⑦.
点评 本题考查基本概念,明确同位素、同素异形体、同分异构体等概念的要点即可解答,难度较小,注重对学生基础知识的考查.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COO-、H+、Na+、K+ | B. | NH4+、OH-、Ba2+、Cl- | ||
| C. | Ca2+、NO3-、Ba2+、K+ | D. | NO3-、Ba2+、H+、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 名称 | 甲烷 | 一氧化碳 | 乙烯 | 苯 | 甲苯 | 苯酚 | 氨水 |

 、
、 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取一定量样品充分干燥,然后将样品加热分解,将产生的气体依次通过盛有无水硫酸铜的干燥管和盛有澄清石灰水的烧瓶 | 若无水硫酸铜不变蓝色,澄清石灰水变浑浊,说明样品全部是PbCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强碱性溶液中:K+、Al3+、Cl-、SO42- | |
| B. | 水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ | |
| C. | 所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+ | |
| D. | 室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com