
| A、反应停止了 |
| B、正反应与逆反应的速率都为零 |
| C、反应物和生成物的浓度相等 |
| D、正反应与逆反应的速率相等且大于0 |


科目:高中化学 来源: 题型:
A、 称量氢氧化钠固体 |
B、 检验铁粉与水蒸气反应产生的氢气 |
C、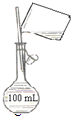 配制150mL 0.10 mol?L-1盐酸 |
D、 分离两种沸点相差较大的液体互溶混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某食盐样品中混有NaI杂质,为测定该食盐样品中NaCl的纯度,甲同学设计的实验过程如下:
某食盐样品中混有NaI杂质,为测定该食盐样品中NaCl的纯度,甲同学设计的实验过程如下:
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,合成这种二肽的氨基酸是
,合成这种二肽的氨基酸是查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓H2SO4 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸钠在水中电离:Na2SO4=Na++SO42- | ||||
B、二氧化锰和浓盐酸共热制氯气的离子方程式:MnO2+4H++4Cl-
| ||||
| C、甲烷燃烧的热化学方程式:CH4+202=CO2+2H2O△H═-889.6kJ?mol-1 | ||||
D、乙烯与水在催化剂、加热条件下反应:CH2═CH2+H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 历史上最早应用的还原性染料是靛蓝,其结构简式如图所示,下列关于靛蓝的叙述中错误的( )
历史上最早应用的还原性染料是靛蓝,其结构简式如图所示,下列关于靛蓝的叙述中错误的( )| A、靛蓝由碳、氢、氧、氮四种元素组成 |
| B、它的分子式是C16H10N2O2 |
| C、该物质是高分子化合物 |
| D、它是芳香族有机物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、K+、OH- |
| B、K+、NH4+、OH- |
| C、Na+、Ca2+、HCO3- |
| D、Fe3+、NO3-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com