
����Ŀ��������һ�־���ǿ�����ԡ���ʴ�Ե�ǿ�ᣬ�仹ԭ����������Ũ�ȵIJ�ͬ���б仯����������˵������Ũ��Խ�ߣ�ƽ��ÿ��������õ��ĵ�����Խ�٣�Ũ����Ļ�ԭ������ҪΪNO2��ϡ����Ļ�ԭ����ΪNO��ʵ�����У�����Cu��ŨHNO3��Ӧ��ȡNO2����Cu��ϡHNO3��Ӧ��ȡNO��
(1)��д��ʵ��������Cu��ϡHNO3��Ӧ��ȡNO�Ļ�ѧ����ʽ����˫���ű������ӵ�ת�Ʒ�����Ŀ_________________
(2)64gCu��������ŨHNO3��Ӧ��ͭȫ�����ú��ռ���22.4L����(��״����)����Ӧ�����ĵ�HNO3�����ʵ�����_________(����ĸ����)��
A.0.5mol B. 1.0mol C. 2.0mol D. 3.0mol
����������ֱ���_______________�������ʵ���֮����_______________
(3)ʵ����������ɱ���ԭΪNO2��NO��Ũ�ȸ�ϡʱ���ỹ���Ա���ԭΪN2O��N2��NH4NO3�ȣ��뽫����3�����ʣ�FeSO4��Fe(NO3)3��Fe2(SO4)3�ֱ����������Ӧ�ĺ����ϣ�����ƽ�÷�Ӧ�Ļ�ѧ����ʽ��___HNO3+_______�� _______+ _______ +___ NO��+___H2O
(4)����Ļ�ԭ����NO��NO2��N2O�ȶԻ������и����ã�Ϊ�˿ɳ�����չ��������������һ���¸���--����ɫ��ѧ������Ҫ��Ӿ��á������ͼ�������ƿ��еĻ�ѧ��Ӧ���������ɵ���ͭ��ȡ����ͭ�ķ��������ҷ��ϡ���ɫ��ѧ������_______(����ĸ����)��
A��Cu![]() Cu(NO3)2
Cu(NO3)2
B��Cu![]() CuO
CuO![]() Cu(NO3)2
Cu(NO3)2
C��Cu![]() CuO
CuO![]() Cu(OH)2
Cu(OH)2![]() Cu(NO3)2
Cu(NO3)2
D��Cu![]() CuSO4
CuSO4![]() Cu(NO3)2
Cu(NO3)2
���𰸡�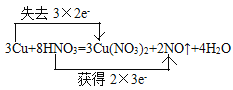 D NO2��NO 1:1 4 3FeSO4 Fe(NO3)3 Fe2(SO4)3 1 2 B
D NO2��NO 1:1 4 3FeSO4 Fe(NO3)3 Fe2(SO4)3 1 2 B
��������
(1)Cu��ϡHNO3��Ӧ��д����ͭ��NO��ˮ������Ԫ�ػ��ϼ����ߵ����ʷ���������Ӧ���������õ����ӣ������������������NԪ�ػ��ϼ۱仯����ת�Ƶ��ӣ�
(2)Cu�����ᷴӦ����Cu(NO3)2��NO2��NO������CuԪ���غ����n[Cu(NO3)2]������NԪ���غ���㷴Ӧ������HNO3�����ʵ�����
(3)�����������У�HNO3�е�Ԫ�ػ��ϼ�λ����ۣ����������ԣ���Ӧ��ԭ����ΪNO���ܽ���ԭ�Ե�FeSO4����ΪFe2(SO4)3��Fe(NO3)3�����ݵ���ת���غ㡢����غ㡢ԭ���غ���ƽ���ӷ���ʽ��
(4)A��ͭ�����ᷴӦ�����һ������������������
B��NԪ�ر���ȫ���ã�û����Ⱦ�����ɣ���;��������ɫ��ѧԭ����
C������ͭ��ˮ����Ӧ��
D��ͭ��ϡ�����Ӧ�������Ƶ�����ͭ��ͭ��Ũ���ᷴӦ����������������塣
(1) Cu��ϡHNO3��Ӧ��������ͭ��һ��������ˮ����ѧ����ʽΪ��3Cu+8HNO3(Ũ)= 3Cu(NO3)2+2NO��+4H2O���÷�Ӧ�У�ͭԪ���ɷ�Ӧǰ����Cu��0�۱�Ϊ��Ӧ��Cu(NO3)2�е�+2�ۣ����ϼ����ߣ�ʧȥ2e-������������Ӧ��NԪ�صĻ��ϼ��ɷ�Ӧǰ�����е�+5�۱�Ϊ��Ӧ��NO�е�+2�����ϼ۽��ͣ����3e-�����ӵ�ʧ��С��������6������Cu��Cu(NO3)2��ϵ��Ϊ3��HNO3��NO��ϵ��Ϊ2�����ڻ���3��Cu(NO3)2�е�6��NO3-û�вμ�������ԭ��Ӧ��Ҳ���������ṩ������HNO3��ϵ����Ϊ2+6=8������HԪ��ԭ���غ㣬��֪ˮ��ϵ��Ϊ4������ʽΪ3Cu+8HNO3=3Cu(NO3)2+2NO��+4H2O ����˫���ŷ���ʾΪ��
 ��
��
(2)n(Cu)=1mol����n[Cu(NO3)2]=1mol��n(NO2)+n(NO)= 22.4L�� 22.4L/mol=1mol��������ԭ����������ʵ���Ϊ1mol������n[Cu(NO3)2]=1mol��֪δ�μ�������ԭ��Ӧ������Ϊ���Ե���������ʵ���Ϊ2mol���ʷ�Ӧ��������������ʵ���Ϊn(HNO3)=1mol+2mol=3mol������ѡ����D��
��Ӧ��Cu���ʵ�����1mol��ʧȥ2mol���ӣ���ʼ����ΪŨ���ᣬ����ԭ����NO2�����ŷ�Ӧ�Ľ��У������Ϊϡ���ᣬ���ᱻ��ԭ��ΪNO������NO2���ʵ���Ϊx����NO���ʵ���Ϊ(1-x)�����ݵ����غ㣬�ɵ�x+3(1-x)=2�����x=0.5mol��1-x=0.5mol���ʶ��ߵ����ʵ����ı�Ϊ1��1��
(3)�����������У�HNO3�е�Ԫ�ػ��ϼ�λ����ۣ����������ԣ���Ӧ��ԭ����ΪNO���ܽ���ԭ�Ե�FeSO4����ΪFe2(SO4)3��Fe(NO3)3�����ݵ����غ㡢ԭ���غ㣬�ɵ÷����ķ�ӦΪ��4HNO3+3FeSO4��Fe(NO3)3+ Fe2(SO4)3+NO��+2H2O��
(4)A��ͭ�����ᷴӦ�����һ�����������������ȴ�����Ⱦ�A����
B��NԪ�ر���ȫ���ã�û����Ⱦ�����ɣ���;��������ɫ��ѧԭ����B��ȷ��
C��������������ͭ��ˮ����Ӧ�������Ƶ�����ͭ��C����
D����;����ͭ��ϡ�����Ӧ�������Ƶ�����ͭ��ͭ��Ũ���ᷴӦ����������������壬��Ⱦ������D����
�ʺ���ѡ����B��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������H2O2�����Ļ��ϼ�Ϊ��1�ۣ�������˫��ˮ��ҽ������������ɱ��������������ϴ�˿ڡ���������A��D�漰H2O2�ķ�Ӧ����д�հף�
A��Na2O2+2HCl===2NaCl+H2O2
B��Ag2O+H2O2===2Ag+O2+H2O
C��2H2O2===2H2O+O2
D��3H2O2+Cr2(SO4)3+10KOH===2K2CrO4+3K2SO4+8H2O
��1��H2O2�����������Եķ�Ӧ��_________������ţ���
��2��H2O2�����������������ֻ�ԭ�Եķ�Ӧ��_________������ţ���
��3����ϡ�����У�KMnO4��H2O2�ܷ���������ԭ��Ӧ��
������Ӧ��H2O2��2e��===2H++O2��
��ԭ��Ӧ��MnO![]() +5e��+8H+===Mn2++4H2O
+5e��+8H+===Mn2++4H2O
д����������ԭ��Ӧ�����ӷ���ʽ��___________________��
��4����K2Cr2O7+14HCl===2KCl+3Cl2��+7H2O+2CrCl3�ķ�Ӧ�У���0.3 mol����ת��ʱ����Cl2�����Ϊ______����״��������������HCl�����ʵ���Ϊ____��
��5����ȥþ���л���������������ܽ⡢_______��������ѧ��Ӧ����ʽΪ___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С���������Լس�ʯ(K2O��Al2O3��6SiO2)Ϊԭ�ϣ���ȡAl2O3��K2CO3�����ʣ������������£�

��1�������ա������������·�Ӧ������
�ټس�ʯ�еĹ�Ԫ����CaCO3������ת��ΪCaSiO3��д��SiO2ת��ΪCaSiO3�Ļ�ѧ����ʽ�� __________��
�ڼس�ʯ�еļ�Ԫ�غ���Ԫ����Na2CO3������ת��Ϊ�����Ե�NaAlO2��KAlO2��д��Al2O3ת��ΪNaAlO2�Ļ�ѧ����ʽ��____________________________________��
��2����ת����ʱ����NaOH����Ҫ������________________________(�����ӷ���ʽ��ʾ)��
��3�����������п���ѭ�����õ���Ҫ������________________��_________________��ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��N2O5��һ��������������һ���¶��·�����Ӧ2N2O5(g)4NO2(g)��O2(g)����H>0, T1�¶��µIJ���ʵ���������±���ʾ��
t/s | 0 | 500 | 1 000 | 1 500 |
c(N2O5)/(mol/L) | 5.00 | 3.52 | 2.50 | 2.50 |
����˵����ȷ����
A. �÷�Ӧ���κ��¶��¾����Է�����
B. T1�¶��µ�ƽ�ⳣ��ΪK1��125��1 000 sʱN2O5(g)ת����Ϊ50%
C. ������������ʱ��T2�¶��·�Ӧ��1 000 sʱ���N2O5(g)Ũ��Ϊ2.98 mol/L����T1<T2
D. T1�¶��µ�ƽ�ⳣ��ΪK1��T2�¶��µ�ƽ�ⳣ��ΪK2����T1>T2����K1<K2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H��һ���������ϵ���Ҫ�ɷ�֮һ����ϳ�·������(���ֲ���Ͳ��ַ�Ӧ������ȥ)��
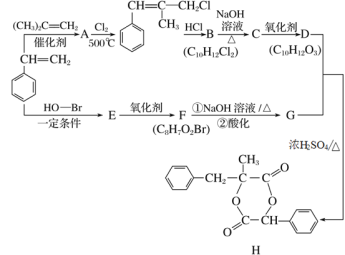
��֪����RCH=CH2+CH2==CHR��![]() CH2=CH2+RCH=CHR�䣻
CH2=CH2+RCH=CHR�䣻
��B�к˴Ź�������ͼ��ʾ��������6�ֲ�ͬ��������ԭ�ӡ�
��ش��������⣺
��1��(CH3)2C=CH2��ͬ���칹���д���˳���칹���л��������Ϊ________��
��2��A�ĺ˴Ź������׳������ϵ�H�⣬����ʾ________��壬�������Ϊ________��
��3��D�����к��еĺ���������������________��E�Ľṹ��ʽΪ__________________��
��4��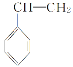 �����Ӿ۷�Ӧ�Ļ�ѧ����ʽΪ____________________________��D��G��Ӧ����H�Ļ�ѧ����ʽΪ_________________________________________��
�����Ӿ۷�Ӧ�Ļ�ѧ����ʽΪ____________________________��D��G��Ӧ����H�Ļ�ѧ����ʽΪ_________________________________________��
��5��G��ͬ���칹���У�ͬʱ����������������________��(�����������칹)��
�ٱ��Ķ�ȡ�������FeCl3��Һ������ɫ��Ӧ���ۺ�����COO�����ṹ
��6�����������ϳ�·�ߣ��Ա�ϩΪԭ��(���Լ���ѡ)������Ʊ�2��3���������ĺϳ�·��_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100 mL NaOH��Һ��ͨ��һ������CO2���壬��ַ�Ӧ������������Һ����μ���0.2 mol/L�����ᣬ����CO2������������������֮���ϵ��ͼ��ʾ��
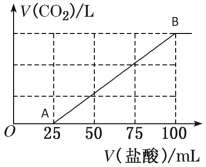
(1)A-B�ε����ӷ�Ӧ����ʽΪ__________________________��
(2)ԭNaOH��Һ��Ũ��Ϊ__________mol/L��
(3)ͨ��CO2�ڱ�״���µ����Ϊ_______mL��
(4)������Һ�����ʳɷ���_______________�������ʵ���֮��Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���� �� ��
A. �ױ��ȿ�ʹ���CCl4��Һ��ɫ��Ҳ��ʹKMnO4������Һ��ɫ
B. �л���![]() ����ȥ������2��
����ȥ������2��
C. �л���A(C4H6O2)�ܷ����Ӿ۷�Ӧ������֪A�Ľṹһ����CH2===CH��COOCH3
D. ������ˮ����ֱ�����͡����Ȼ�̼������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��ѧ�м��ֳ������ʵ�ת����ϵ����ͼ��ʾ

��D��Һ�����ˮ�пɵõ���FΪ��ɢ�ʵĺ��ɫ���壮��ش��������⣺
��1�����ɫ������F����ֱ����С�ķ�Χ��________.
��2��A��B��H�Ļ�ѧʽ��A__________��B__________�� H________.
��3����H2O2���ӵĵ���ʽΪ______________��
��д��C��������Һ��˫��ˮ��Ӧ�����ӷ���ʽ�� _______________________��
��4��д������E�������ӵ�ʵ�鷽��������_______________________��
��5����C��Һ�м�����C�����ʵ�����Na 2 O 2 ��ǡ��ʹCת��ΪF��д���÷�Ӧ�����ӷ���ʽ��____________________________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com