
写出下列反应的离子反应方程式(全对得10分,有错即为0分)
(1)NaAlO2溶液中加入少量的盐酸
(2)AlCl3溶液中加入过量的NaOH
(3)Al2O3与NaOH水溶液的反应
(4)Fe3O4溶解在稀盐酸中
(5)FeCl2溶液中加入酸化的H2O2溶液
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
在一次兴趣小组活动中,一小组利用物质间的互变,设计成一平面“魔方”如图所示。已知:
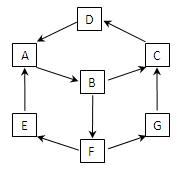
①A、B、C、D、G含有同种元素。
②E是通常情况下密度最小的气体;B与硝酸银溶液反
应生成不溶于稀硝酸的白色沉淀;B也能将一种能形成酸
雨的氧化物氧化为F,F是一种含氧酸,且F的稀溶液
能与A反应生成E和G。
| 物质 | 纯A(单质) | B(溶液) | D(固体) | G(溶液) |
| 颜色 | 银白色 | 黄色 | 红棕色 | 浅绿色 |
③几种物质的部分物理性质:
依据以上信息填空:
(1)G生成C的过程中所出现的现象为 ;
(2)写出下列反应的化学方程式:
A→B : ;
(3)写出下列反应的离子方程式:
B→F: ;
酸性条件下,G与次氯酸溶液反应: ;
(4)使一定质量的Zn与100mL18.5 mol·L-1 酸F的浓溶液充分反应,Zn完全溶解,同时生成标准状况下的气体A 33.6L。将反应后的溶液稀释至1L,测得溶液中c(H+)=0.1mol·L-1,则气体A的成份及体积比为 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年甘肃省高三上学期期末考试(理综)化学部分 题型:填空题
在一次兴趣小组活动中,一小组利用物质间的互变,设计成一平面“魔方”如图所示。已知:

①A、B、C、D、G含有同种元素。
②E是通常情况下密度最小的气体;B与硝酸银溶液反
应生成不溶于稀硝酸的白色沉淀;B也能将一种能形成酸
雨的氧化物氧化为F,F是一种含氧酸,且F的稀溶液
能与A反应生成E和G。
|
物质 |
纯A(单质) |
B(溶液) |
D(固体) |
G(溶液) |
|
颜色 |
银白色 |
黄色 |
红棕色 |
浅绿色 |
③几种物质的部分物理性质:
依据以上信息填空:
(1)G生成C的过程中所出现的现象为 ;
(2)写出下列反应的化学方程式:
A→B : ;
(3)写出下列反应的离子方程式:
B→F: ;
酸性条件下,G与次氯酸溶液反应: ;
(4)使一定质量的Zn与100mL18.5 mol·L-1 酸F的浓溶液充分反应,Zn完全溶解,同时生成标准状况下的气体A 33.6L。将反应后的溶液稀释至1L,测得溶液中c(H+)=0.1mol·L-1,则气体A的成份及体积比为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com