
(9分)
(1)实验室中可用KClO3和浓HCl反应制取氯气,写出该反应的化学方程式,并用双线桥法标出电子转移的方向和数目 ;该反应中,氧化产物是 ,还原产物是 ,氧化产物与还原产物的物质的量之比是 。
(2)化学镀镍的溶液中含有Ni2+和H2PO2-在酸性条件下发生如下反应,请配平该反应。
Ni2++ H2PO2-+ → Ni++ H2PO3-+
科目:高中化学 来源:2016届浙江省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列关于氧化物的各项叙述正确的是
①酸性氧化物肯定是非金属氧化物 ②非金属氧化物肯定是酸性氧化物 ③碱性氧化物肯定是金属氧化物 ④金属氧化物都是碱性氧化物 ⑤酸性氧化物均可与水反应生成相应的酸 ⑥与水反应生成酸的氧化物不一定是酸酐,与水反应生成碱的氧化物不一定是碱性氧化物 ⑦不能跟酸反应的氧化物一定能跟碱反应
A.①②③④ B.⑤⑥⑦ C.②③⑥⑦ D.③⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上第一次月考化学试卷(解析版) 题型:填空题
(10分)(1)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出热量649.5 中kJ,其热化学方程为 。
又已知:H2O(l)=H2O(g);ΔH=+44.0kJ/mol。则11.2L(标准状况)乙硼烷完全燃烧生成气态水时放出的热量为 。
恒温、恒压(1.01×105Pa)下,将2.0molSO2与amolO2的混合气体通入一个容积可变的密闭容器中,发生如下反应:2SO2(g)+O2(g) 2SO3(g);ΔH<0
2SO3(g);ΔH<0
(2)T1℃下反应达平衡时,测得容器内n(SO3)=1.3mol,n(O2)=3.0mol,则a=__________;平衡时SO2的转化率为_________。T2℃下反应达平衡时,混合气体的物质的量共为4.8mol.T1与T2的关系是________(选填序号)。
①T1>T2 ②T1<T2 ③T1=T2
查看答案和解析>>
科目:高中化学 来源:2016届福建省大田市高三上学期第一次月考化学试卷(解析版) 题型:选择题
市场上销售的“84”消毒液,其商品标识上有如下叙述:①本品为无色液体,呈碱性②使用时加水稀释③可对餐具、衣物进行消毒,可漂白浅色衣物。其有效成分可能是
A. Cl2 B. SO2 C. NaClO D. KMn04
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰市宁城县高三上学期第一次统考化学试卷(解析版) 题型:填空题
煤是一种重要的化工原料,人们将利用煤制取的水煤气、焦炭、甲醚等广泛用于工农业生产中。
(1)已知:
①C(s)+H2O(g)═CO(g)+H2(g) △H=+131.3kJ·mol﹣1
②CO2(g)+H2(g)═CO(g)+H2O(g) △H=+41.3kJ·mol﹣1
则碳与水蒸气反应生成二氧化碳和氢气的热化学方程式为 。
该反应在 (填“高温”、“低温”或“任何温度”)下有利于正向自发进行.
(2)有人利用炭还原法处理氮氧化物,发生反应C(s)+2NO(g) N2(g)+CO2(g).向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如下表所示:
N2(g)+CO2(g).向某密闭容器中加入一定量的活性炭和NO,在T1℃时,不同时间测得各物质的浓度如下表所示:
| 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
①10~20min内,N2的平均反应速率v(N2)= .
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是__________(填字母序号).
A.通入一定量的NO B.加入一定量的活性炭
C.加入合适的催化剂 D.适当缩小容器的体积
(3)研究表明:反应CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
H2(g)+CO2(g)平衡常数随温度的变化如下表所示:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
若反应在500℃时进行,设起始时CO和H2O的浓度均为0.020mol·L﹣1,在该条件下达到平衡时,CO的转化率为 .
(4)用CO做燃料电池电解CuSO4溶液、FeCl3和FeCl2混合液的示意图如图1所示,其中A、B、D均为石墨电极,C为铜电极.工作一段时间后,断开K,此时A、B两极上产生的气体体积相同.
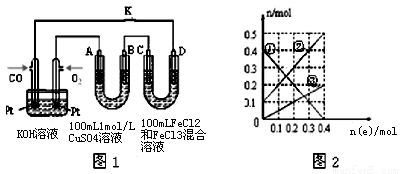
①乙中A极产生的气体在标准状况下的体积为 .
②丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图2所示,则图中③线表示的是 (填离子符号)的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要 mL 5.0mol·L﹣1 NaOH溶液.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上学期第一次月考化学试卷(解析版) 题型:选择题
对于可逆反应:C(s)+CO2(g) 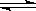 2CO(g),在一定温度下其平衡常数为K。下列条件的变化中,能使K值发生变化的是
2CO(g),在一定温度下其平衡常数为K。下列条件的变化中,能使K值发生变化的是
A.将C(s)的表面积增大 B.增大体系的压强
C.升高体系的温度 D.使用合适的催化剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列各组离子在满足指定条件下,能大量共存的是
A.无色溶液:Cu2+、K+、Cl-、CO32-
B.使酚酞显红色的溶液:Mg2+、Fe2+、Cl-、SO42-
C.加Fe粉能产生H2的溶液:Ba2+、Na+、Cl-、SO42-
D.加盐酸能产生气体的溶液:Na+、K+、NO3-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2016届浙江省宁波市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列各项中,理由、结论及因果关系均正确的是
选项 | 理由 | 结论 |
A | 键能:N≡N>Cl-Cl | 单质沸点:N2>Cl2 |
B | 分子中可电离的H+个数:H2SO4>CH3COOH | 酸性:H2SO4>CH3COOH |
C | 元素的金属性:K>Na | 碱性:KOH>NaOH |
D | 氧化性:Fe3+>Cu2+ | 还原性:Fe2+>Cu |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省许昌、襄城、长葛三校高一上期中测试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.物质所含元素的化合价越高,氧化性越强
B.物质失去电子数目越多,还原性越强
C.元素由化合态变为游离态,该元素一定被还原
D.置换反应一定有电子转移
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com