
液氨与纯水相似,也存在着微弱的电离:2NH3 NH4+ + NH2—,据此判断以下叙述中错误的是
NH4+ + NH2—,据此判断以下叙述中错误的是
A.NH3、NH4+、NH—的电子数相等,化学性质也相同
B.一定温度下液氨中c(NH4+)·c(NH2—)是一个常数
C.液氨的电离达到平衡时c(NH3)≠c(NH4+)=c(NH2—)
D.加入其他物质,c(NH4+)/c(NH2—)可能不变
科目:高中化学 来源:2017届安徽省江淮十校高三11月质检化学试卷(解析版) 题型:选择题
a b c d e f g h I j k l
A. 含砂粒的食盐水过滤,选用a、d、f、l
B. 萃取水中碘,选用b、c、d、f
C. 将胆矾转化为CuSO4固体,选用g、h、j、l
D. 检验滤液中的Fe3+,选用d、f、h、i
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上期中化学卷(解析版) 题型:选择题
25 ℃时,Ksp[Mg(OH)2] = 5.61×10-12,Ksp(MgF2)= 7.42×10-11。下列说法正确的是( )
A.25 ℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大
B. 25 ℃时,Mg(OH)2固体在20 mL 0.01 mol/L氨水中的 Ksp比在20 mL 0.01 mol/L NH4Cl溶液中的Ksp小
Ksp比在20 mL 0.01 mol/L NH4Cl溶液中的Ksp小
C.25 ℃时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大
D.25 ℃时,在Mg(OH)2的悬浊液加入NaF溶液后,Mg(OH)2不可能转化成为MgF2
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上学期第三次质检化学试卷(解析版) 题型:选择题
一定温度下,在三个恒容体积均为2.0L的容器中发生反应:PCl5(g) 
 PCl3(g)+Cl2(g),下列说法正确的是
PCl3(g)+Cl2(g),下列说法正确的是
编号 | 温度(℃) | 起始/mol | 平衡/mol | 达到平衡 所需时间/s | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
Ⅱ | 320 | 0.80 | t2 | ||
Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
A.平衡常数K:容器Ⅱ>容器Ⅲ
B.反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ
C.反应到达平衡时,容器I中的平均速率为v(PCl5)=0.1/t1 mol•L-1•s-1
D.起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl3 0.45 mol和Cl2 0.10 mol,则反应将向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上学期第三次质检化学试卷(解析版) 题型:选择题
下列措施有利于反应:N2(g)+3H2(g) 2NH3(g)△H=-92kJ•mol-1平衡
2NH3(g)△H=-92kJ•mol-1平衡 向正反应方向移动的是
向正反应方向移动的是
①升高温度 ②降低温度 ③增大压强 ④减小压强 ⑤增大NH3浓度 ⑥减小NH3浓度
A.②④⑥ B.①③⑥ C.②③⑤ D.② ③⑥
③⑥
查看答案和解析>>
科目:高中化学 来源:2017届山东省日照市高三上学期期中化学试卷(解析版) 题型:填空题
工业合成氨:N2(g)+3H2(g) 2NH3(g) △H<0,氨又可以进一步制各硝酸,在工业上一般可进行连续生产。请回答下列问题:
2NH3(g) △H<0,氨又可以进一步制各硝酸,在工业上一般可进行连续生产。请回答下列问题:
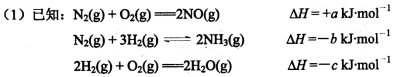
若有68g氨气经催化氧化完全生成NO(g)和H2O(g)所放出的热量为___________KJ。
(2)合成氨反应达到平衡后,某时刻改变下列选项中的__________条件,在达到新平衡的过程中逆反应速率始终增大。
a.升温 b.缩小容积 c.增大c(N2) d .使用催化剂
.使用催化剂
(3)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对合成氨反应的影响。实验结果如下图所示:(图中T表示温度,横轴表示起始时H2的物质的量,纵轴表示平衡时NH3的体积分数)
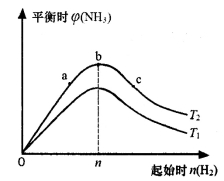
图像中T1和T2的关系是:T1____________T2 (填“>”“<”或“=”)。
比较在a、b、c三点所处的平衡状态中,反应物N 2的转化率最大的是_______________(填字母)。
2的转化率最大的是_______________(填字母)。
③若容器容积为1L,b点对应的起始时n(H2)=0.30mol,测得平衡时H2的转化率为60%,则平衡时c(N2)为_________________mo1·L-1。(已知反应物的物质的量按n(H2):n(N2)=3:1投料时,平衡时NH3的体积分数最大)
(4)一定温度下,将2mol N2和4mol H2置于1L的恒容密闭容器中反应,测得不同温度(T)、不同时间段内工业合成氨反应中N2的转化率,得到数据如下表所示:
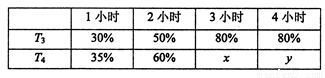
上表中x、y的大小关系为x_____________y。(填“>”“=”“<”“≥”或“≤” )
)
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期第三次月考化学试卷(解析版) 题型:选择题
O2F2可以发生反应:H2S+4O2F2=SF6+2HF+4O2,下列说法正确的是( )
A.氧气是氧化产物
B.O2F2既是氧化剂又是还原剂
C.若生成4.48LHF,则转移0.8mol电子
D.还原剂与氧化剂的物质的量之比为1:4
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:填空题
研究大气中含硫化合物(主要是SO2和H2S)的转化具有重要意义。
(1)高湿条件下,写出大气中SO2转化为HSO3-的方程式:__________;____________。
(2)土壤中的微生物可将大气中H2S经两步反应氧化成SO42-,两步反应的能量变化示意图如下:
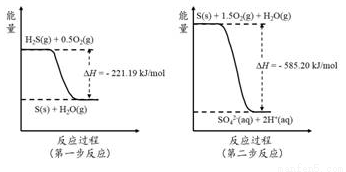
1mol H2S(g)全部氧化成SO42-(aq)的热化学方程式为_________________________。
(3)二氧化硫—空气质子交换膜燃料电池可以利用大气所含SO2快速启动,其装置示意图如下:
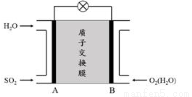
①质子的流动方向为_________________(“从A到B”或“从B到A”)。
②负极的电极反应式为__________________________。
(4)燃煤烟气的脱硫减排是减少大气中含硫化合物污染的关键。SO2烟气脱除的一种工业流程如下:
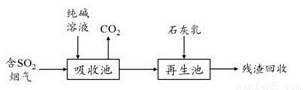
① 用纯碱溶液吸收SO2将其转化为HSO3-,反应的离子方程式是________________。
② 若石灰乳过量,将其产物再排回吸收池,其中可用于吸收SO2的物质的化学式是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com