
把500mLNH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含a mol氢氧化钠的溶液恰好反应完全,另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为()
A. 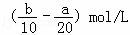 B. (2b﹣a)mol/L C.
B. (2b﹣a)mol/L C. 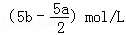 D. (10b﹣5a)mol/L
D. (10b﹣5a)mol/L
考点: 有关混合物反应的计算.
专题: 守恒法.
分析: NH4HCO3和Na2CO3的混合溶液加入NaOH,反应为NH4HCO3+2NaOH═NH3•H20+Na2CO3+H2O,加入含b mol HCl的盐酸的反应为NH4HCO3+HCl═NH4Cl+CO2↑+H2O,Na2CO3+2HCl═2NaCl+H2O+CO2↑,根据方程式计算.
解答: 解:设100ml溶液中含有NH4HCO3xmol,Na2CO3ymol,
NH4HCO3和Na2CO3的混合溶液加入NaOH,反应为NH4HCO3+2NaOH═NH3•H20+Na2CO3+H2O,
则NH4HCO3为0.5amol,
加入含b mol HCl的盐酸的反应为NH4HCO3+HCl═NH4Cl+CO2↑+H2O,Na2CO3+2HCl═2NaCl+H2O+CO2↑,
则Na2CO3的物质的量为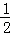 ×(b﹣0.5a)mol,
×(b﹣0.5a)mol,
n((Na+)=2n(Na2CO3)=(b﹣0.5a)mol,
c(Na+)=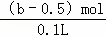 =(10b﹣5a)mol/L,
=(10b﹣5a)mol/L,
故选D.
点评: 本题考查混合物的计算,题目难度不大,本题注意用守恒的方法根据化学方程式计算.


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:
硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、漂白粉等一系列物质(见图).下列说法正确的是()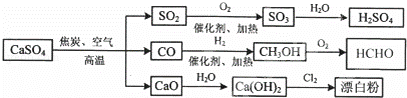
A. CO、SO2、SO3均是酸性氧化物
B. 除去与水反应,图示转化反应均为氧化还原反应
C. 工业上利用Cl2和澄清石灰水反应来制取漂白粉
D. 用CO合成CH3OH进而合成HCHO的两步反应,原子利用率均为100%
查看答案和解析>>
科目:高中化学 来源: 题型:
对实验Ⅰ~Ⅳ的实验现象预测正确的是()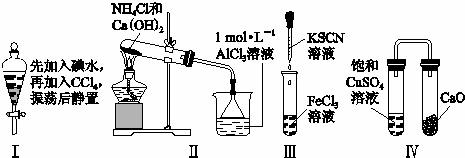
A. 实验Ⅰ:液体分层,下层呈无色
B. 实验Ⅱ:烧杯中先出现白色沉淀,后溶解
C. 实验Ⅲ:试管中产生血红色沉淀
D. 实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
铁及其化合物在生产和生活中有着广泛的应用.
(1)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:
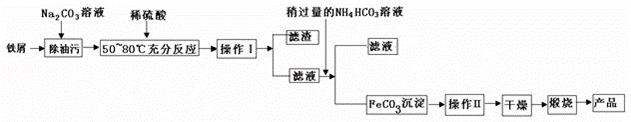
回答下列问题:
①操作Ⅰ、Ⅱ的名称分别是 、 .
②写出在空气中煅烧FeCO3的化学方程式 ;
③煅烧如果不充分,产品中将有Fe2+存在,试设计实验检验产品中有无Fe2+.
(2)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定.
a.称取2.850g绿矾(FeSO4•7H2O)产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.
①写出酸性KMnO4溶液与FeSO4溶液反应的离子方程式
②计算上述样品中FeSO4•7H2O的质量分数为 已知M(FeSO4•7H2O)=278g/mol]
③滴定达到终点时锥形瓶中溶液颜色变化为
④下列操作会导致样品中FeSO4•7H2O的质量分数的测定结果偏高的有 .
a.未干燥锥形瓶
b.盛装标准液的滴定管没有用标准液润洗
c. 滴定终点时滴定管尖嘴中产生气泡
d.量取待测液,视线注视刻度时开始平视、结束俯视.
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列叙述中完全正确的一组是( )
①常温常压下,1mol甲基(﹣CH3)所含的电子数为10NA
②由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极生成0.2gH2,则电路中通过电子0.2NA
③5.6g铁粉与硝酸反应失去的电子数一定是0.3NA
④常温常压下,16gO2和O3的混合物中所含的原子数为NA
⑤1molC10H22分子中共价键总数为31NA
⑥1molCl2发生反应时,转移的电子数一定是2NA.
A. ②③④ B. ②③⑥ C. ①②④⑤ D. ②④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
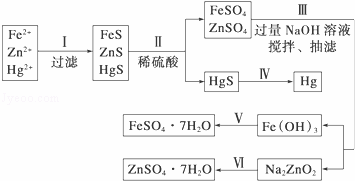
某工厂排出的污水中含有大量的Fe3+、Zn2+、Hg2+三种金属离子.以下是某化学研究性学习小组的同学设计除去污水中的金属离子,并回收绿矾、皓矾(ZnSO4•7H2O)和汞的方案.
NaOH溶液、硫化钠溶液、硫化亚铁、稀硫酸、铁粉
如图
(1)步骤Ⅱ所发生反应的离子方程 .
步骤Ⅲ中抽滤的目的是 ,该步骤产生Fe(OH)3的反应的离子方程式为 .
(3)步骤Ⅵ中得到硫酸锌溶液的离子方程式为 .
(4)欲实现步骤Ⅴ,需加入的试剂有 、 ,所涉及的主要操作依次为 .
(5)步骤Ⅳ常用的方法是 ,该步骤是否对环境有影响? (填“是”或“否”),如有影响,请你设计一个绿色环保方案来实现步骤Ⅳ的反应: .
(6)该研究小组的同学在强碱溶液中,用次氯酸钠与Fe(OH)3反应获得了高效净水剂Na2FeO4,该反应的离子方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com