

| 实验序号 | 盐酸标准液体积(mL) | 所消耗氢氧化钠标准液的体积(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.50 | 20.70 |
| 2 | 20.00 | 2.00 | 22.00 |
| 3 | 20.00 | 1.00 | 20.80 |
分析 (1)酸式滴定管下端有玻璃活塞;
(2)为了便于判断滴定终点,要观察锥形瓶中颜色变化;
(3)锥形瓶装液前不能润洗;根据根据c(碱)=$\frac{c(酸)×V(酸)}{V(碱)}$判断不当操作对相关物理量的影响;
(4)锥形瓶中盛放的是盐酸,所以滴定时溶液的pH逐渐增大;
(5)先判断数据的合理性,然后求出NaOH溶液的平均体积,然后根据HCl~NaOH求NaOH溶液的物质的量浓度.
解答 解:(1)酸式滴定管下端有玻璃活塞,由图可知b为酸式滴定管;
故答案为:b;
(2)为了便于判断滴定终点,眼睛要观察锥形瓶中颜色变化,根据颜色变化判断滴定终点;
故答案为:a;
(3)锥形瓶装液前不能润洗,若锥形瓶用待测液润洗,待测液的物质的量偏多,造成V(酸)增大,根据c(碱)=$\frac{c(酸)×V(酸)}{V(碱)}$可知,c(碱)偏高,
故答案为:偏高;
(4)锥形瓶中盛放的是盐酸,所以滴定时溶液的pH逐渐增大,由图可知a曲线符合;
故答案为:a;
(5)三次消耗的氢氧化钠溶液的体积为20.20mL,20.00mL,19.80mL均有效,则NaOH溶液的平均体积为$\frac{20.20mL+20.00mL+19.80mL}{3}$=20.00mL,
c(碱)=$\frac{c(酸)×V(酸)}{V(碱)}$=$\frac{20.00mL×0.1000mol/L}{20.00mL}$=0.10mol/L;
故答案为:0.10.
点评 本题考查中和滴定的操作以及误差分析,题目难度中等,明确中和滴定实验的仪器、步骤、指示剂的选择、数据处理等即可解答,侧重于考查学生的实验能力和数据处理能力.


科目:高中化学 来源: 题型:选择题
| A. | 加成→消去→取代 | B. | 消去→加成→水解 | C. | 取代→消去→加成 | D. | 消去→加成→消去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 )加氢产物1,2-二甲基环乙烷(
)加氢产物1,2-二甲基环乙烷( )的一氯代产物有(不考虑立体异构)( )
)的一氯代产物有(不考虑立体异构)( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KAl(SO4)2 | B. | NH4Al(SO4)2 | C. | (NH4)2Fe(SO4)2 | D. | NH4Fe(SO4)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
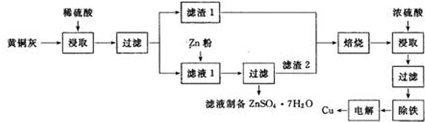 铜是一种重要的有色金属,近些年来铜的用途越来越广泛.铜矿有辉铜矿(主要成分为Cu2S)、斑铜矿(主要成分为Cu5FeS4)、蓝铜矿[主要成分为Cu2(OH)2CO3]及黄铜矿(主要成分为CuFeS2)等.
铜是一种重要的有色金属,近些年来铜的用途越来越广泛.铜矿有辉铜矿(主要成分为Cu2S)、斑铜矿(主要成分为Cu5FeS4)、蓝铜矿[主要成分为Cu2(OH)2CO3]及黄铜矿(主要成分为CuFeS2)等.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属元素的原子最外层电子数都大于或等于4 | |
| B. | 只有非金属能形成含氧酸或含氧酸盐 | |
| C. | Na2O2中阴阳离子的个数比为1:1 | |
| D. | 非金属元素组成的化合物不一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3 PH3 AsH3 SbH3 | B. | Si SiC H2O CO2 | ||
| C. | NaI NaBr NaCl NaF | D. | Li Na K Rb |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 溶液 | 操作及现象 |
| A | Ca(OH)2溶液 | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失.再加入足量NaOH溶液,又变浑浊. |
| B | 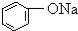 溶液 溶液 | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失. |
| C | Ca(ClO)2溶液 | 通入CO2,溶液没有明显变化.再滴入品红溶液,红色褪去. |
| D | CaCl2溶液 | 通入CO2,溶液没有明显变化.若同时通入CO2和NH3,则溶液变浑浊. |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
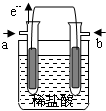 某研究小组提出了一种新的设想:利用原电池原理,设计一种H2、Cl2燃料电池,原电池总反应为:H2+Cl2=2HCl,在对外提供电能的同时还可得到工业上具有重要用途的较浓的盐酸.他们设计的原电池装置如下,其中两个电极均为多孔铂电极.下列有关叙述不正确的是( )
某研究小组提出了一种新的设想:利用原电池原理,设计一种H2、Cl2燃料电池,原电池总反应为:H2+Cl2=2HCl,在对外提供电能的同时还可得到工业上具有重要用途的较浓的盐酸.他们设计的原电池装置如下,其中两个电极均为多孔铂电极.下列有关叙述不正确的是( )| A. | a为负极,通入的气体为氢气 | |
| B. | 正极的电极反应式为:Cl2+2e-=2Cl- | |
| C. | 电流由b极流出,经外电路到a极 | |
| D. | 原电池内部,H+移向负极,Cl-移向正极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com