
【题目】氨气是重要的化工原料。
(1)检验氨气极易溶于水的简单操作是:收集一试管氨气,______________。
(2)往饱和食盐水中依次通入足量的NH3和足量的CO2,生成沉淀的化学式为_________;过滤后,使余液尽可能析出较多NH4Cl晶体的方法是:再通入足量的NH3、冷却并加入________,请说明这样操作为什么可以析出较多NH4Cl的原因:_________________。某NaHCO3晶体中含有NaCl杂质,某同学在测定其中NaHCO3的含量时,称取5.000g试样,定容成100mL溶液,用标准盐酸溶液滴定(用甲基橙做指示剂),测定数据记录如下:
滴定次数 | 待测液(mL) | 0.5000mol/L盐酸溶液的体积(mL) | |
初读数 | 终读数 | ||
第一次 | 20.00 | 1.00 | 21.00 |
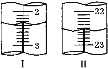
第二次 | 20.00 | 如图Ⅰ | 如图Ⅱ |
(3)定容过程中需要用到的仪器有烧杯、玻璃棒、___________和____________。
(4)当滴定至__________________________,即为滴定终点;第二次滴定,从图I图II显示消耗的盐酸溶液体积为_________mL。
(5)该实验测定样品中NaHCO3的质量分数为__________(保留2位小数)。
(6)若该同学测定结果偏大,请写出一个造成该误差的原因_____________。
【答案】倒插入水中,水迅速充满试管 NaHCO3 NaCl 足量的NH3、冷却并加入NaCl,能够增大NH4+和Cl-的浓度,使平衡NH4Cl(s)NH4+(aq)+Cl-(aq)逆向移动 100mL容量瓶 胶头滴管 溶液由橙色变成黄色,且半分钟内部变色 20.20 84.42% 滴定管用蒸馏水洗涤后,直接注入标准酸液进行滴定(或滴定前有气泡,滴定后气泡消失或锥形瓶用待测液润洗了等)
【解析】
(1)根据氨气极易溶于水分析解答;
(2)根据侯氏制碱法的反应原理分析判断;结合NH4Cl饱和溶液中存在NH4Cl(s)NH4+(aq)+Cl-(aq)的平衡分析解答;
(3)根据定容的操作分析解答;
(4) 碳酸氢钠溶液显碱性,用甲基橙做指示剂时,开始时溶液显橙色,解甲基橙的变色范围分析判断;根据滴定管的结构结合图I图II读出初读数和终读数,再计算消耗的盐酸溶液体积;
(5)计算两次消耗盐酸的平均值,计算消耗盐酸的物质的量,依据方程式:HCl+NaHCO3=NaCl+H2O+CO2↑,然后计算碳酸氢钠的物质的量和质量,计算其质量分数;
(6)根据c(待测)=![]() ,测定结果偏大,造成该误差的原因为V(标准)偏大,结合造成V(标准)偏大的可能因素解答。
,测定结果偏大,造成该误差的原因为V(标准)偏大,结合造成V(标准)偏大的可能因素解答。
(1)检验氨气易溶于水的简单操作是:收集一试管氨气,将试管倒插入水中,水迅速充满试管,故答案为:倒插入水中,水迅速充满试管;
(2)根据侯氏制碱法的反应原理,往饱和食盐水中依次通入足量的NH3和足量的CO2,可生成碳酸氢钠沉淀;NH4Cl饱和溶液中存在NH4Cl(s)NH4+(aq)+Cl-(aq),为尽可能析出较多NH4Cl晶体,可以向溶液中再通入足量的NH3、冷却并加入NaCl,可使平衡逆向移动,故答案为:NaHCO3;NH3;NaCl;足量的NH3、冷却并加入NaCl,能够增大NH4+和Cl-的浓度,使平衡NH4Cl(s)NH4+(aq)+Cl-(aq)逆向移动;
(3)定容过程中需要用到的仪器有烧杯、玻璃棒、100mL容量瓶和胶头滴管,故答案为:100mL容量瓶;胶头滴管;
(4) 用甲基橙做指示剂,用标准盐酸溶液滴定NaHCO3,碳酸氢钠溶液显碱性,开始时溶液显橙色,当滴入最后一滴盐酸,溶液由橙色变成黄色,且半分钟内部变色,即为滴定终点;根据图I图II,初读数为2.40 mL,终读数为22.60mL,则消耗的盐酸溶液体积20.20 mL,故答案为:溶液由橙色变成黄色,且半分钟内部变色;20.20 ;
(5)第一次消耗盐酸的体积是21.00mL-1.00mL=20.00mL,所以两次消耗盐酸的平均值是![]() =20.10mL,所以消耗盐酸的物质的量是0.0201L×0.5000mol/L;根据方程式HCl+NaHCO3=NaCl+H2O+CO2↑可知,碳酸氢钠的物质的量是0.0201L×0.5000mol/L,质量是0.0201L×0.5000mol/L×84g/mol,所以碳酸氢钠的纯度是
=20.10mL,所以消耗盐酸的物质的量是0.0201L×0.5000mol/L;根据方程式HCl+NaHCO3=NaCl+H2O+CO2↑可知,碳酸氢钠的物质的量是0.0201L×0.5000mol/L,质量是0.0201L×0.5000mol/L×84g/mol,所以碳酸氢钠的纯度是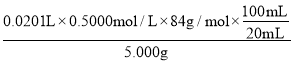 ×100%=84.42%,故答案为:84.42%;
×100%=84.42%,故答案为:84.42%;
(6)若该同学测定结果偏大,造成该误差的原因可能是滴定管用蒸馏水洗涤后,直接注入标准酸液进行滴定(或滴定前有气泡,滴定后气泡消失或锥形瓶用待测液润洗了等),故答案为:滴定管用蒸馏水洗涤后,直接注入标准酸液进行滴定(或滴定前有气泡,滴定后气泡消失或锥形瓶用待测液润洗了等)。


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:
【题目】白桦脂酸对白血病等恶性肿瘤细胞有抑制作用,其结构简式如图所示,在白桦脂酸中加入合适的试剂检验其官能团(必要时可加热),下列试剂、现象、结论都正确的一项是

选项 | 试剂 | 现象 | 结论 |
A | 氯化铁溶液 | 溶液变色 | 含有羟基 |
B | 银氨溶液 | 有银镜产生 | 含有醛基 |
C | 碳酸氢钠溶液 | 有气泡产生 | 含有羧基 |
D | 酸性KMnO4溶液 | 溶液褪色 | 含有碳碳双键 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.0kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:
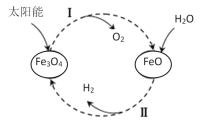
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2kJ/mol
过程Ⅱ:……
下列说法不正确的是( )
A.过程Ⅰ中每消耗232gFe3O4转移2mol电子
B.过程Ⅱ热化学方程式为:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=-128.9kJ/mol
C.过程Ⅰ、Ⅱ中能量转化的形式依次是:太阳能→化学能→热能
D.铁氧化合物循环制H2具有成本低、产物易分离等优点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)文明中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的价电子排布式为_________,3d能级上的未成对的电子数为______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中SO42-的立体构型是_____。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为______ ,提供空轨道的中心微粒是_____。
③氨的沸点_____(“高于”或“低于”)膦(PH3),原因是______;氨是_____分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______。
(3)单质铜及镍都是由______键形成的晶体:元素铜与镍的第二电离能分别为:ICu=1958kJ/mol,INi=1753kJ/mol,ICu>INi的原因是______。
(4)某镍白铜合金的立方晶胞结构如图所示。
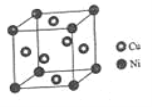
①晶胞中镍原子与铜原子的数量比为_____。
②若合金的密度为dg/cm3,晶胞参数a=________nm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M是一种常用香料的主要成分之一,其合成路线如下。
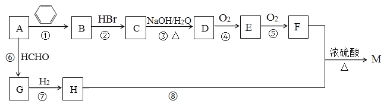
已知:
①相同条件下1体积烃A完全燃烧消耗4体积氧气;
②RC≡CH+HCHO![]() RC≡CCH2OH;
RC≡CCH2OH;
③反应①的原子利用率为100%,反应类型属于加成反应;
④M的分子式为C13H18O2。
回答下列问题:
(1)A的名称为___________;G分子中有___ _个碳原子在同一条直线上。
(2)反应②~⑧中属于加成反应的是______;H中官能团的名称为___________。
(3)物质M的结构简式为____________。B的一种同类别异构体存在顺反异构,该物质发生加聚反应生成的高分子化合物的结构简式为_____________。
(4)反应③的化学反应方程式为_______________。
(5)符合下列条件的F的同分异构体共有_____种。
①能发生银镜反应;②能发生水解反应;③属于芳香族化合物。
其中核磁共振氢谱为4组峰,且峰面积之比为6∶2∶1∶1的为 (任写一种物质的结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机合成工厂以植物秸秆或木材为初始原料经过生物发酵,制备聚酯纤维H和医药中间体E,其合成路线如下图所示:
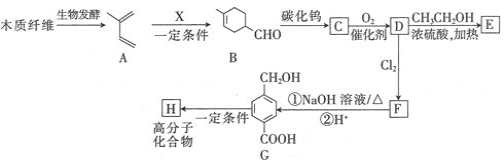
已知:①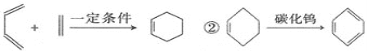
回答下列问题:
(1)A的化学名称是________;B所含官能团的名称是________。
(2)X的结构简式________;G→H的反应类型是________。
(3)D→E的化学方程式________。
(4)符合下列条件的G同分异构体共有________种;其中核磁共振氢谱有五组峰的结构简式________。
①能发生银镜反应;②能与FeCl3溶液发生显色反应;③能发生水解反应。
(5)参照上述合成路线,利用CH2=CH-CH=CH2为初始原料设计合成![]() 的路线_______________。
的路线_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是![]()
![]() 氧化还原反应的实质是电子的转移
氧化还原反应的实质是电子的转移
![]() 若1mol气体的体积为
若1mol气体的体积为![]() ,则它一定处于标准状况下
,则它一定处于标准状况下
![]() 标准状况下,1LHCl和1L
标准状况下,1LHCl和1L![]() 的物质的量相同
的物质的量相同
![]() 溶于水得到的溶液可以导电的化合物就是电解质
溶于水得到的溶液可以导电的化合物就是电解质
![]() 利用丁达尔现象区别溶液和胶体
利用丁达尔现象区别溶液和胶体
![]() 两种物质的物质的量相同,则它们在标准状况下的体积也相同
两种物质的物质的量相同,则它们在标准状况下的体积也相同
![]() 在同温、同体积时,气体物质的物质的量越大,则压强越大
在同温、同体积时,气体物质的物质的量越大,则压强越大
![]() 同温同压下,气体的密度与气体的相对分子质量成正比
同温同压下,气体的密度与气体的相对分子质量成正比
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中可以获得淡水、食盐,并可提取镁和溴等物质。
(1)海水淡化的方法有_______(填一种)。
(2)写出元素钠在元素周期表中的位置:_______。
(3)从海水中提取镁的流程如下图所示:
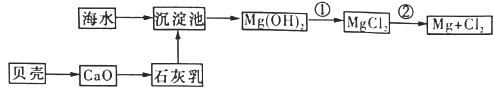
反应①的离子方程式为_______________。
反应②的化学方程式为_______________。
(4)从海水中提取溴的主要步骤是向浓缩的海水中通人氯气,将溴离子氧化,该反应的离子方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】沼气的主要成分是CH4,还含有CO2、H2S等。Jo De Vrieze等设计了利用膜电解法脱除沼气中的CO2和H2S,并将阴极处理后气体制成高纯度生物甲烷,其流程如图所示。
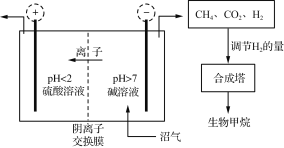
(1) 需控制电解槽中阴极室pH>7,其目的是________________。
(2) 阳极室逸出CO2和________(填化学式);H2S在阳极上转化为SO42-而除去,其电极反应式为___________________。
(3) 在合成塔中主要发生的反应为:
反应Ⅰ: CO2(g)+4H2(g)=CH4(g)+2H2O(g) ΔH1
反应Ⅱ: CO2(g)+H2(g)=CO(g)+H2O(g) ΔH2
调节![]() =4,充入合成塔,当气体总压强为0.1 MPa,平衡时各物质的物质的量分数如图1所示;不同压强时,CO2的平衡转化率如图2所示:
=4,充入合成塔,当气体总压强为0.1 MPa,平衡时各物质的物质的量分数如图1所示;不同压强时,CO2的平衡转化率如图2所示:
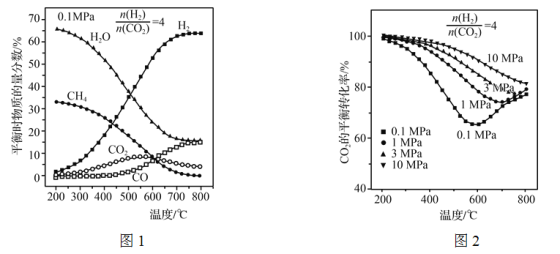
①反应CO2(g)+CH4(g)=2CO(g)+2H2(g)的△H=________(用ΔH1、ΔH2表示)。
②图1中,200~550 ℃时,CO2的物质的量分数随温度升高而增大的原因是__________。
③图2中,相同温度下,压强越大,CO2的平衡转化率越大,其原因是___________________;在压强为10 MPa时,当温度在200~800 ℃范围内,随温度升高,CO2的平衡转化率始终减小,其原因是________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com