
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
| A、容器①、②中反应的平衡常数相等 |
| B、平衡时,两个容器中NH3的体积分数相等 |
| C、容器②中达平衡时放出的热量Q=23.15 kJ |
| D、若容器①体积为0.5 L,则平衡时放出的热大于23.15 kJ |
| 2mol×23.15KJ |
| 92.6KJ |
| 0.5mol |
| 0.75mol+2.25mol+0.5mol |
| 1 |
| 7 |


科目:高中化学 来源: 题型:
| A、油脂能在酸性溶液中水解生成高级脂肪酸,可用于防止油脂变质 |
| B、铝的熔点很高,可用于制作耐高温材料 |
| C、浓硫酸具有吸水性,可用于干燥氨气、二氧化碳等气体 |
| D、过氧化钠能与二氧化碳反应产生氧气,可用于高空飞行或潜水的供氧剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
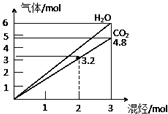 两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是( )| A、②⑤ | B、②④ | C、③④ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、鼓励农民将秋后农作物秸秆焚烧 |
| B、用杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,作家庭燃气 |
| C、限制燃油汽车数量的增加 |
| D、将煤进行脱硫处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com