
����Ŀ���������ӷ�Ӧ����ʽ��ȷ����(����)
A. ��̼����þ��Һ�м�������Ca(OH)2��Һ�� Mg2����HCO![]() ��Ca2����2OH��===MgCO3����CaCO3����2H2O
��Ca2����2OH��===MgCO3����CaCO3����2H2O
B. ���Ȼ�������Һ��ϡ��������3Fe2����4H����NO![]() ===3Fe3����2H2O��NO��
===3Fe3����2H2O��NO��
C. ��̼������Һͨ������Ķ�����̼������CO![]() ��CO2��H2O===2HCO
��CO2��H2O===2HCO![]()
D. ��������Һ����μ���Ba(OH)2��Һ��Al3���պó�����ȫ�� Al3����SO![]() ��Ba2����3OH��===BaSO4����Al(OH)3��
��Ba2����3OH��===BaSO4����Al(OH)3��
���𰸡�B
��������A����̼����þ��Һ�м�������Ca��OH��2��Һ�����ӷ�ӦΪMg2++2HCO3-+2Ca2++4OH-�TMg��OH��2��+CaCO3��+2H2O����A����B�����Ȼ�������Һ��ϡ�����ϵ����ӷ�ӦΪ3Fe2++4H++NO3-�T3Fe3++2H2O+NO������B��ȷ��C����̼������Һͨ������Ķ�����̼��������ӷ�ӦΪ2Na++CO32-+CO2+H2O�T2NaHCO3������C����D����������Һ����μ���Ba��OH��2��Һ��Al3+�պó�����ȫ�����ӷ�ӦΪ2Al3++3SO42-+3Ba2++6OH-�T3BaSO4��+2Al��OH��3������D����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���G��һ�ֳ��õ�ֲ���ζ�ͣ��ɰ�����·�ߺϳɣ�

��֪��![]()
�ش��������⣺
(1)���й�����ϩ��˵������ȷ����_________������ĸ����
a.����������ԭ�ӹ�ƽ��
b.�ܷ���������Ӧ�����ܷ�����ԭ��Ӧ
c.�ܷ����Ӿ۷�Ӧ���ɸ߷���
d.��ʹ���Ը��������Һ��ɫ
(2)��F����G�ķ�Ӧ����Ϊ_________________________��
(3)C�й����ŵ�����Ϊ___________����C����D�ķ�Ӧ����Ϊ___________��
(4)D�Ļ�ѧ����Ϊ___________����D����E�Ļ�ѧ����ʽΪ___________��
(5)�����Ϻ�������ȡ�������ҷ����к���������F��ͬ���칹����_________�֣����к˴Ź���������ʾ������壬�ҷ����֮��Ϊ3:2:2:3����__________����ṹ��ʽ����
(6)���������ϳ�·�ߣ������BΪԭ�ϣ����Լ���ѡ���Ʊ�����ˮ����֬![]() �ĺϳ�·�ߣ�________________��
�ĺϳ�·�ߣ�________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ������˿�� Cl2��2Fe+3Cl2 ![]() 2FeCl3��Ϊԭ�Ͻ�����������ʵ�顣����ѡ����ȷ����( )
2FeCl3��Ϊԭ�Ͻ�����������ʵ�顣����ѡ����ȷ����( )
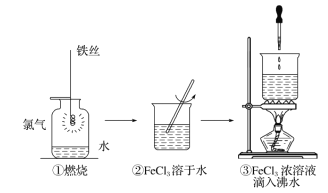
A. ʵ������ ����Ӧ�Ƶõ����ʾ�Ϊ������
B. ʵ�����еķ�Ӧ����������ԭ��Ӧ���������ֻ�����Ӧ�����еķ�Ӧ
C. ʵ������ѧ����ʽΪ FeCl3+3H2O==Fe(OH)3��+3HCl
D. ʵ������ �����漰�����ʾ�Ϊ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�����Ϊ��������ȱ�������涨��ʳ���б�����������ĵ���ء�����ʳ�����Ƿ�ӵ⣬���������·�Ӧ��
KIO3+ KI+ H2SO4�T K2SO4+ I2 + H2O
��1����ƽ�÷���ʽ��������˫���ŷ���ʾ�÷���ʽ����ת�Ƶķ�������Ŀ��____________________
��2���÷�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ______________��
��3�������Ӧ��ת��0.5mol���ӣ�������I2�����ʵ���Ϊ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƣ�NaNO2����һ����Ҫ�Ĺ�ҵ�Σ�Ҳ���������ࡢ�����ʳƷ��Ⱦɫ�ͷ�����������ˮ�������Ҵ�. ij��ѧ��ȤС����������ƽ��ж�Ƕ�̽����
i.�������Ƶ��Ʊ�
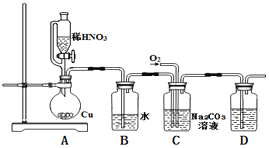
��1��ʵ�����ú�ѹ��Һ©���������ͨ��Һ©�����������ŵ���____��
��2��D�г���ʯ��ˮ����ǣ���C���Ʊ�NaNO2�����ӷ���ʽΪ_______________��
ii. ̽���������������ᷴӦ�������ɷ֣�
��֪����NO+NO2+2OH���T2NO2��+H2O ������Һ�����¶ȣ�NO2��21�棬NO����152��
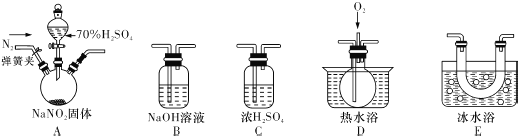
��3����ӦǰӦ���ɼУ���ͨ��һ��ʱ�䵪����Ŀ����___________��
��4��Ϊ�˼���װ��A�����ɵ�����������������˳����������ӣ���
A��C��______��______��______��
��5���ڹرյ��ɼУ���Һ©������������70%�����A�в�������ɫ���壮
��ȷ��A�в��������庬��NO�����ݵ�������_________________��
��װ��B��������____________________��
iii. ���ʵ��֤������������NaNO2���������ԣ�___________��
��ѡ�õ��Լ���NaNO2��Һ��KMnO4��Һ��FeSO4��Һ��KI��Һ��ϡ���ᡢ������Һ��KSCN��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ï��[(C5H5)2Fe]����һ�����������Ӻ�2������ϩ�������ӹ��ɣ����ķ��ֿ���˵���л������������о��о�����̱�������¼����������˽����л��������о��������ٽ��˽����л���ѧ�ķ�չ����ï�������û�ԭ�����뻷���ϩ�ڵ�����Χ�з�����Ӧ���Ƶá�
��ش��������⣺
��1����ï�����۵���173��(��100��ʱ��ʼ����)���е���2.19�棬������ˮ�������ڱ������ѵȷǼ����ܼ����ݴ˿��ƶ϶�ï������Ϊ______���壬�ɴ˿ɽ�һ����֪���ڶ�ï���ṹ�У�![]() ��Fe2+֮���γɵĻ�ѧ��������_______��
��Fe2+֮���γɵĻ�ѧ��������_______��
��2����д�������ʵ����Ļ����ϩ���巴Ӧ��������ѧ����ʽ____________��
��H2C=CH��C��C��CH3�ǻ����ϩ��һ��ͬ���칹�壬������ӽṹ�д���ͬһƽ���ϵ�ԭ�Ӹ��������______����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鲻��������
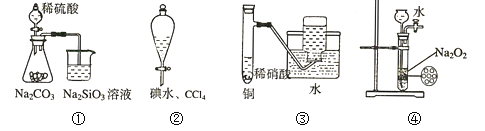
A. װ������֤��Ԫ�طǽ�����ǿ�� S��C��Si
B. װ���������Ȼ�̼��ȡ��ˮ�еĵ�
C. װ�������Ʊ����ռ�����NO����
D. װ�������Ʊ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У��������
A. ����Ũ���ᡢŨ���Ṳ�Ȳ�����55��60�淴Ӧ����������
B. ������ʹ���Ը��������ɫ��˵��������û��̼̼˫��
C. �����л��е���ϩ��������ˮ��ȥ
D. ҽԺ��75%�ƾ�ɱ����������75%��ָ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ķ��ֻ������ڹ�ҵ������Ҫ��Ӧ�á�
��1�������������ƣ�Na2S2O4���ֳƱ��շۣ������ʺ�ľ����ֽ��Ư������ˮ��Һ���ʲ��ȶ����м�ǿ�Ļ�ԭ�ԡ�
��Na2S2O4��SԪ�صĻ��ϼ�Ϊ__________��
��Na2S2O4��¶�ڿ�����������������ˮ���������ʣ�������Ӧʱ�����������ͻ�ԭ�������ʵ���֮��Ϊl��2ʱ������Ϊ___________���ѧʽ����
�۽������NaOH��Һ��ϣ���ͨ��SO2���壬��õ����շۣ���ʱ���ᱻ����ΪCO2���÷�Ӧ�Ļ�ѧ����ʽΪ____________________��
��2��������ɻ�����Ⱦ��ij���Է�ˮ�к���Cr2O72-������ʱ���ý��������ƣ�Na2S2O5����Cr2O72-ת��Ϊ���Խϵ͵�Cr3+���ٵ���pH��8��ʹ��Ԫ�س����������������÷�ˮ��Cr3+Ũ��Ϊ0.52mg��L-1���ﵽ�ŷű���
��Na2S2O5�μӷ�Ӧ�����ӷ���ʽΪ____________��
�ڴ�����ķ�ˮ��Cr3+�����ʵ���Ũ��Ϊ__________mol��L-1��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com