
 ĄūÓƵēµ¼ĀŹ“«øŠĘ÷æÉ»ęÖʵēµ¼ĀŹĒśĻßĶ¼£¬ĻĀĶ¼ĪŖÓĆ0.1mol•L-1NaOHČÜŅŗµĪ¶Ø10mL£¬0.1mol•L-1ŃĪĖį¹ż³ĢÖŠµÄµēµ¼ĀŹĒśĻߣ®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©
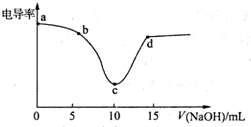
ĄūÓƵēµ¼ĀŹ“«øŠĘ÷æÉ»ęÖʵēµ¼ĀŹĒśĻßĶ¼£¬ĻĀĶ¼ĪŖÓĆ0.1mol•L-1NaOHČÜŅŗµĪ¶Ø10mL£¬0.1mol•L-1ŃĪĖį¹ż³ĢÖŠµÄµēµ¼ĀŹĒśĻߣ®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©| A£® | µēµ¼ĀŹ“«øŠĘ÷ÄÜÓĆÓŚÅŠ¶ĻĖį¼īÖŠŗĶµĪ¶ØµÄÖÕµć | |
| B£® | øĆ¹ż³ĢÖŠ£¬aµćĖłŹ¾ČÜŅŗµÄµ¼µēŠŌ×īĒæ | |
| C£® | cµćµēµ¼ĀŹ×īŠ”ŹĒŅņĪŖ“ĖŹ±ČÜŅŗÖŠµ¼µēĪ¢Į£µÄŹżÄæ×īÉŁ | |
| D£® | dµćĖłŹ¾ČÜŅŗÖŠ“ęŌŚ£ŗc£ØCl-£©+c£ØOH-£©=c£ØH+£©+c£ØNa+£© |
·ÖĪö A£®HClŗĶNaOH·“Ó¦·½³ĢŹ½ĪŖHCl+NaOH=NaCl+H2O£¬øł¾ŻĶ¼ĻóÖŖ£¬“Ó0-10mLÖ®¼ä£¬Ėę×Å·“Ó¦µÄ½ųŠŠ£¬ČÜŅŗÖŠc£ØH+£©ÅضČÖš½„¼õŠ”£¬ČÜŅŗµÄµēµ¼ĀŹÖš½„½µµĶ£¬¼ÓČėČÜŅŗĢå»ż“óÓŚ15mLŹ±£¬ČÜŅŗÖŠĒāŃõøłĄė×ÓÅضČÖš½„Ōö“ó£¬ČÜŅŗµÄµēµ¼ĀŹŌö“ó£¬øł¾ŻĶ¼ÖŖ£¬µ±Ē”ŗĆÖŠŗĶŹ±µēµ¼ĀŹ×īŠ”£»
B£®µēµ¼ĀŹÓėµ¼µēŠŌ³ÉÕż±Č£»
C£®ČÜŅŗµēµ¼ĀŹÓėĄė×ÓÅØ¶Č³ÉÕż±Č£¬cµćµēµ¼ĀŹµĶŹĒŅņĪŖĄė×ÓÅØ¶ČŠ”£»
D£®ČĪŗĪµē½āÖŹČÜŅŗÖŠ¶¼“ęŌŚµēŗÉŹŲŗć£®
½ā“š ½ā£ŗA£®HClŗĶNaOH·“Ó¦·½³ĢŹ½ĪŖHCl+NaOH=NaCl+H2O£¬øł¾ŻĶ¼ĻóÖŖ£¬“Ó0-10mLÖ®¼ä£¬Ėę×Å·“Ó¦µÄ½ųŠŠ£¬ČÜŅŗÖŠc£ØH+£©ÅضČÖš½„¼õŠ”£¬ČÜŅŗµÄµēµ¼ĀŹÖš½„½µµĶ£¬¼ÓČėČÜŅŗĢå»ż“óÓŚ15mLŹ±£¬ČÜŅŗÖŠĒāŃõøłĄė×ÓÅضČÖš½„Ōö“ó£¬ČÜŅŗµÄµēµ¼ĀŹŌö“ó£¬øł¾ŻĶ¼ÖŖµ±Ē”ŗĆÖŠŗĶŹ±µēµ¼ĀŹ×īŠ”£¬ĖłŅŌæÉŅŌµēµ¼ĀŹ“«øŠĘ÷ÄÜÓĆÓŚĖį¼īÖŠŗĶµĪ¶ØÖÕµćµÄÅŠ¶Ļ£¬¹ŹAÕżČ·£»
B£®µēµ¼ĀŹÓėµ¼µēŠŌ³ÉÕż±Č£¬øł¾ŻĶ¼ÖŖøƵćµēµ¼ĀŹ×ī“ó£¬ĖłŅŌĘäµ¼µēŠŌ×īĒ棬¹ŹBÕżČ·£»
C£®ČÜŅŗµēµ¼ĀŹÓėĄė×ÓÅØ¶Č³ÉÕż±Č£¬cµćµēµ¼ĀŹµĶŹĒŅņĪŖĄė×ÓÅØ¶ČŠ”£¬¶ų²»ŹĒµ¼µēĪ¢Į£ŹżÄæ×īÉŁ£¬¹ŹC“ķĪó£»
D£®ČĪŗĪµē½āÖŹČÜŅŗÖŠ¶¼“ęŌŚµēŗÉŹŲŗć£¬øł¾ŻµēŗÉŹŲŗćµĆc£ØCl-£©+c£ØOH-£©=c£ØH+£©+c£ØNa+£©£¬¹ŹDÕżČ·£»
¹ŹŃ”C£®
µćĘĄ ±¾ĢāŅŌµē½āÖŹČÜŅŗµÄµ¼µēŠŌĪŖŌŲĢåæ¼²éĖį¼ī»ģŗĻČÜŅŗ¶ØŠŌÅŠ¶Ļ£¬Ć÷Č··“Ó¦ŹµÖŹ”¢µēµ¼ĀŹµÄÓ°ĻģŅņĖŲ¼°»ģŗĻČÜŅŗÖŠČÜÖŹŹĒ½ā±¾Ģā¹Ų¼ü£¬»įøł¾ŻĶ¼ĻóÖŠĒśĻß±ä»Æ»ńČ”ŠÅĻ¢”¢¼Ó¹¤ŠÅĻ¢£¬“Ó¶ųĄūÓĆŠÅĻ¢“šĢā£¬×¢Ņāµē½āÖŹČÜŅŗÖŠµēŗÉŹŲŗćÓėČÜŅŗĖį¼īŠŌĪŽ¹Ų”¢ÓėČÜŅŗÅضČĪŽ¹Ų£¬ĪŖŅדķµć£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆ½¹ĢæŌŚµēĀÆÖŠ»¹Ō¶žŃõ»Æ¹čÖĘČ”¹čµ„ÖŹ | |
| B£® | ÓĆĆŗĢæ×÷Č¼ĮĻ·¢µē | |
| C£® | ÓĆĢśæóŹÆĮ¶Ģś | |
| D£® | ÓĆ“æ¼īÖĘ²£Į§ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO”śCO2 | B£® | CO2”śNa2CO3 | C£® | NO2”śHNO3 | D£® | S”śCuS |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ¼×“¼æÉ×÷ĪŖČ¼ĮĻµē³ŲµÄŌĮĻ£®ŅŌCH4ŗĶH2OĪŖŌĮĻ£¬ĶعżĻĀĮŠ·“Ó¦Ą“Öʱø¼×“¼£®
¼×“¼æÉ×÷ĪŖČ¼ĮĻµē³ŲµÄŌĮĻ£®ŅŌCH4ŗĶH2OĪŖŌĮĻ£¬ĶعżĻĀĮŠ·“Ó¦Ą“Öʱø¼×“¼£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČŻĘ÷ÖŠæÉÄÜÓŠ¹ĢĢ岊Ōü | B£® | ĖłµĆČÜŅŗÖŠŅ»¶Ø“ęŌŚFe2+ | ||
| C£® | ·“Ó¦¹ż³ĢÖŠĖ®µÄµēĄė³Ģ¶ČŌö“ó | D£® | ŌŁ¼ÓČėĶŗó£¬ČÜŅŗŗģÉ«Öš½„ĶĖČ„ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | CH3-CH=CH2 | B£® | CH2=CH2 | C£® | C2H6 | D£® | C6H6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £ØÓƵē×ÓŹ½±ķŹ¾£©£®
£ØÓƵē×ÓŹ½±ķŹ¾£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¹żŃõ»ÆÄĘÓėĖ®·“Ó¦£ŗ2O22-+2H2OØTO2”ü+4OH- | |
| B£® | NaOHČÜŅŗÓėNH4ClČÜŅŗ¹²ČČ£ŗOH-+NH4+$\frac{\underline{\;\;”÷\;\;}}{\;}$NH3”ü+H2O | |
| C£® | Cl2ÓėĖ®·“Ó¦£ŗCl2+H2OØTCl-+ClO-+2H+ | |
| D£® | FeCl3ČÜŅŗæĢŹ“ĶµēĀ·°å£ŗFe3++CuØTCu2++Fe2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com