
| A. | H2SO4 | B. | NH4Cl | C. | CH3COONa | D. | NaOH |
分析 物质能促进水的电离,且溶液显碱性说明物质是含弱离子的盐溶液,水解促进水的电离,溶液呈碱性说明是弱酸阴离子水解显碱性.
解答 解:A、H2SO4溶液是酸溶液,氢离子浓度抑制水的电离,溶液中的氢离子浓度增大显酸性,故A错误;
B、氯化铵是弱碱强酸盐,铵根离子水解呈酸性,促进水的电离,溶液中氢离子浓度增大,故B错误;
C、CH3COONa是强碱弱酸盐,醋酸根离子水解呈碱性,促进水的电离,溶液中氢氧根离子浓度增大,故C正确;
D、NaOH溶液是强碱溶液,氢氧根离子抑制水的电离,溶液中氢离子浓度减小,故D错误,
故选C.
点评 本题考查了盐类水解的分析判断,水的电离平衡的影响因素分析,题目较简单.


科目:高中化学 来源: 题型:解答题
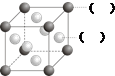 A、B、C、D、E、F为前四周期的元素.其中,A元素和B元素的原子都有一个未成对电子,A3+比B-少一个电子层,B原子得一个电子后3p轨道全充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解性在同族元素所形成的氢化物中最大;D的最高化合价与最低化合价代数和为4,其最高价氧化物对应的水化物可以用于制取炸药和制作铅蓄电池;E元素的基态原子核外有六种运动状态的电子;F元素的单质为红色固体,可通过“湿法冶金”而得.请回答下列问题:
A、B、C、D、E、F为前四周期的元素.其中,A元素和B元素的原子都有一个未成对电子,A3+比B-少一个电子层,B原子得一个电子后3p轨道全充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解性在同族元素所形成的氢化物中最大;D的最高化合价与最低化合价代数和为4,其最高价氧化物对应的水化物可以用于制取炸药和制作铅蓄电池;E元素的基态原子核外有六种运动状态的电子;F元素的单质为红色固体,可通过“湿法冶金”而得.请回答下列问题: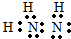 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
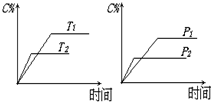 可逆反应mA(固)+nB(气)?e C(气)+f D(气)△H,反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图:下列叙述正确的是( )
可逆反应mA(固)+nB(气)?e C(气)+f D(气)△H,反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图:下列叙述正确的是( )| A. | 达平衡后,加入催化剂则C%增大 | |
| B. | 达平衡后,增加A的量有利于平衡向右移动 | |
| C. | 化学方程式中n>e+f | |
| D. | 达平衡后升温,则平衡向左移动,且△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-,AlO2-,SO32-,Na+ | B. | NO3-,CH3COO-,Na+,NH4+ | ||
| C. | Cl-,NO3-,Mg2+,K+ | D. | SO42-,HCO3-,Cl-,K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3mol/(L•min) | B. | 0.6mol/(L•min) | C. | 0.9mol/(L•min) | D. | 1.2mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体的浓度不再变化 | B. | 容器内压强不再改变 | ||
| C. | 气体的分子数不再变化 | D. | 各气体的浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 同浓度下列溶液中:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl,④NH3•H2O,c(NH4+)由大到小的顺序是:①>③>②>④ | |
| B. | 常温时,将等体积的盐酸和氨水混合后pH=7,则c (NH4+)>c (Cl-) | |
| C. | 0.2 mol•L-1Na2CO3溶液中:c (CO32-)+c (HCO3-)+c (H2CO3)=0.2 mol•L-1 | |
| D. | 向醋酸钠溶液中加入适量醋酸,得到酸性溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com