
| A. | 14g乙烯和甲烷混合气体中的氢原子数一定大于2NA | |
| B. | 2molN2与6molH2在一定条件下反应生成的NH3 分子数一定大于2NA | |
| C. | 56gFe溶于过量稀硝酸,电子转移数一定等于3NA | |
| D. | 标准状况下,2.24 LCH3Cl含有的共价键数一定小于4NA |
分析 A、当14g全部为乙烯时,含2mol氢原子;
B、合成氨的反应为可逆反应;
C、铁和过量硝酸反应后变为+3价;
D、标况下一氯甲烷为气体.
解答 解:A、当14g全部为乙烯时,含2mol氢原子,而甲烷中H元素的百分含量高于乙烯,故当14g为乙烯和甲烷的混合物时,含有的H原子个数一定大于2NA个,故A正确;
B、合成氨的反应为可逆反应,故不能进行彻底,则生成的氨气分子个数小于2NA个,故B错误;
C、铁和过量硝酸反应后变为+3价,故56g铁即1mol铁转移的电子数为3NA个,故C正确;
D、标况下2.24L一氯甲烷的物质的量为0.1mol,故含0.4NA条共价键,即小于4NA条,故D正确.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
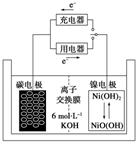 一种碳纳米管能够吸附氢气,用这种材料制备的二次电池原理如图所示,该电池的电解质为6mol•L-1KOH溶液,下列说法中正确的是( )
一种碳纳米管能够吸附氢气,用这种材料制备的二次电池原理如图所示,该电池的电解质为6mol•L-1KOH溶液,下列说法中正确的是( )| A. | 放电时电池正极的电极反应为:NiO(OH)+H2O+e-═Ni(OH)2+OH- | |
| B. | 放电时K+移向负极 | |
| C. | 放电时电池负极的电极反应为H2-2e-═2H+ | |
| D. | 该电池充电时将碳电极与电源的正极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖银镜反应实验后的试管内壁附有银,可用氨水清洗 | |
| B. | 氢氧化铁胶体在直流电场中,一段时间阴极附近红褐色加深,说明胶体带正电 | |
| C. | 用标准酸溶液滴定未知碱溶液时,盛装待测溶液的锥形瓶不需要用待测溶液润洗 | |
| D. | 测定溶液pH的操作:将湿润的pH试纸置于表面皿上,用玻璃棒蘸取溶液,点在试纸中部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铜与盐酸反应:O2-+2H+=H2O | |
| B. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+CO2+H2O=CaCO3+2HClO | |
| C. | 大理石跟盐酸反应:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| D. | 醋酸和氨水反应:H++OH-=H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2mol钠与过量盐酸反应生成NA个H2分子 | |
| B. | 金属钠加到冷水中,反应的离子方程式是:Na+2H2O═Na++OH-+H2↑ | |
| C. | 1molNa2O2与足量的水反应,转移电子数为2NA个 | |
| D. | 为测定熔融NaOH的导电性,可在瓷坩埚中熔化NaOH固体后进行测量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | Na2S溶液中:SO42-、K+、Cl-、Cu2+ | |
| C. | 0.1 mol•L-1 NH4HCO3溶液中:K+、Na+、NO3-、Cl- | |
| D. | 在溶质为KNO3和NaHSO4的溶液中:Fe2+、Ca2+、Al3+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com