
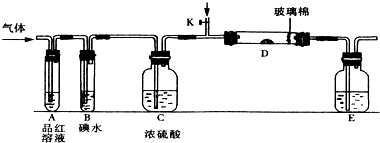
分析 实验探究SO2和Cl2的性质:装置A:品红溶液验证漂白性,二氧化硫、氯水都能使其褪色,B装置:二氧化硫与碘水中的碘反应,检验二氧化硫的还原性,装置C:浓硫酸干燥二氧化硫,装置D:二氧化硫与氧气发生催化氧化,若D中盛铜粉,氯气和铜反应生成氯化铜,装置E:吸收尾气,吸收多余的SO2和Cl2可用氢氧化钠溶液吸收.
(1)①二氧化硫具有漂白性和有机色素结合为不稳定的化合物,氯气通入溶液中与水反应生成的次氯酸具有漂白性,可以氧化有机色素为无色;
②铜粉在Cl2中加热Cu粉红热,并生成产生棕黄色烟氯化铜;
③若装置D中装的是五氧化二钒(催化剂),二氧化硫催化氧化为三氧化硫;
④二氧化硫具有还原性和碘单质发生氧化还原反应生成硫酸和氢碘酸;
(2)足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量物质可以看到白色沉淀产生;
A.氨水和二氧化硫反应生成亚硫酸铵,亚硫酸根离子和钡离子结合生成沉淀;
B.稀盐酸不和二氧化硫反应不能生成沉淀;
C.稀硝酸溶液具有强氧化性,将二氧化硫氧化成硫酸根,结合钡离子生成沉淀;
D.氯化钙溶液和二氧化硫不反应;
(3)先根据X中元素的质量之比求出原子个数之比,再根据题中反应现象判断该反应生成的离子,由氧化还原反应写出离子方程式.
解答 解:(1)①二氧化硫能和有色物质反应生成无色物质,所以二氧化硫有漂白性;氯气和水反应生成次氯酸,次氯酸具有强氧化性,能使有色物质褪色,所以若从左端分别通入SO2和Cl2,装置A中观察到的现象相同,都使品红褪色,但本质不同,
故答案为:不相同;
②铜粉在Cl2中加热,铜被氯气氧化,Cu粉红热,并生成产生棕黄色烟氯化铜,
故答案为:Cu粉红热,并产生棕黄色烟;
③二氧化硫和氧气在五氧化二钒作催化剂、加热条件下能发生氧化还原反应生成三氧化硫,反应方程式为 2SO2+O2 $?_{△}^{催化剂}$2SO3,
故答案为:2SO2+O2 $?_{△}^{催化剂}$2SO3;
④SO2通入B装置碘水中,溶液颜色退去,发生了氧化还原反应:碘单质具有氧化性,二氧化硫具有还原性,被碘单质氧化为硫酸,本身被还原为碘化氢,反应的离子方程式为:SO2+I2+2H2O=4H++2I-+SO42-,
故答案为:SO2+I2+2H2O=4H++2I-+SO42-;
(2)将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量试剂仍然无法观察到沉淀产生,说明不发生反应:
A、氨水加入后生成亚硫酸铵,亚硫酸根和钡离子生成沉淀,故A正确;
B、稀盐酸加入后不反应,故B错误;
C、稀硝酸溶液具有强氧化性,将二氧化硫氧化成硫酸根,与钡离子生成硫酸钡沉淀,故C正确;
D.氯化钙溶液和二氧化硫不反应,故D错误;
故答案为:AC;
(2)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3,所以X中S和O的原子个数比为$\frac{4}{32}$:$\frac{3}{16}$=2:3,所以该离子为S2O3 2-;氯气有强氧化性,能和硫代硫酸根离子发生氧化还原反应,根据题意知,该反应中有硫酸根离子生成,所以氯气中氯元素得电子生成氯离子,所以该反应的离子方程式为:Cl2+H20+S2O32-=SO42-+S↓+2Cl-+2H+,
故答案为:Cl2+H20+S2O32-=SO42-+S↓+2Cl-+2H+.
点评 本题考查了性质实验方案的设计,明确二氧化硫的性质是解本题关键,会根据二氧化硫的性质分析装置中各个装置的作用及发生的反应,注意稀硝酸有强氧化性而氧化二氧化硫,为易错点,试题有利于培养学生的分析、理解能力及化学实验能力,题目难度中等.


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 放电时,锂铝合金作负极,Li+向负极移动 | |
| B. | 充电时,阴极的电极反应式为:Fe+2Li2S-4e-=4Li++FeS2 | |
| C. | 该电池可用LiCl水溶液作电解质溶液 | |
| D. | 以Al作阳极,FeS为阴极,LiCl-KCl低共熔混合物为电解质进行电解,可以制得FeS2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.时间/h 熔出率 温度 | 1.5 | 2.5 | 3.0 | 3.5 | 4.0 |
| 800℃ | 0.054 | 0.091 | 0.127 | 0.149 | 0.165 |
| 830℃ | 0.481 | 0.575 | 0.626 | 0.669 | 0.685 |
| 860℃ | 0.515 | 0.624 | 0.671 | 0.690 | 0.689 |
| 950℃ | 0.669 | 0.711 | 0.713 | 0.714 | 0.714 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素代号 | A | B | C | D | E | F | G | H |
| 原子半径/pm | 37 | 160 | 70 | 66 | 186 | 143 | 104 | 99 |
| 最高化合价 | +1 | +2 | +5 | +1 | +3 | +6 | +7 | |
| 最低化合价 | -3 | -2 | -2 | -1 |
 ,B、H两种元素形成化合物的电子式是
,B、H两种元素形成化合物的电子式是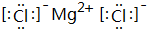 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
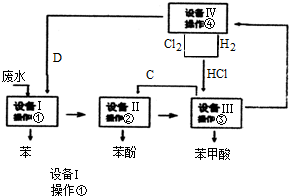
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 的烃X,红外光谱和核磁共振表明其分子中氢原子的化学环境只有一种,根据分析,下列说法中不正确的是( )
的烃X,红外光谱和核磁共振表明其分子中氢原子的化学环境只有一种,根据分析,下列说法中不正确的是( )| A. | X的分子式为C5H4 | |
| B. | X中碳原子的化学环境有2种 | |
| C. | 1 mol X在一定条件下可与2 mol氢气发生反应 | |
| D. | X不能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
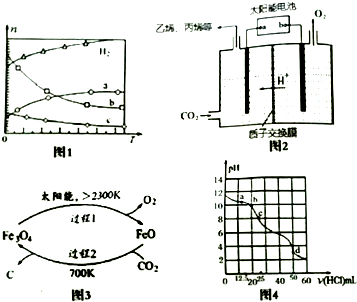
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10s-15sC(NH3)增加量等于0.25 mol/L | |
| B. | 化学反应速率的关系是3v正(H2)=2v正(NH3) | |
| C. | 达到平衡后,分离出少量NH3,平衡正向移动,v正增大 | |
| D. | 保持压强不变充入Ar气体,v正减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)?N2O4(g)(无色),如图所示.
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)?N2O4(g)(无色),如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com