
| A. | 从海水中提炼出的氘(含 HDO 0.03‰)进行核聚变,放出巨大的能量以解决能源问题, 成为一条新的科学思路.HDO与 H2O化学性质相同 | |
| B. | 从海水中提取镁可以采用下列方法:海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{HCl}{→}$MgCl2溶液→MgCl2•6H2O$→_{△}^{HCl}$MgCl2(熔融)$\stackrel{电解}{→}$Mg | |
| C. | 从海水获得的碘,可以跟氧气反应生成多种化合物,其中一种称为碘酸碘,已知该化合物中碘元素呈+3和+5两种价态,则这种化合物的化学式是 I4O9 | |
| D. | 除去粗盐中的 SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
分析 A.同位素是质子数相同,中子数不同的同种元素的不同原子,原子最外层电子数相同,化学性质相同;
B.海水中含有镁离子,先将海水蒸发、浓缩得到含有镁离子的溶液,再向溶液中加入沉淀剂将Mg 2+转化为Mg(OH)2,将Mg(OH)2溶于稀盐酸得到MgCl2,将MgCl2在HCl氛围中加热得到MgCl2固体,电解熔融MgCl2得到Mg;
C.根据化合物的名称为碘酸碘,而碘酸碘的化学式一定为Im(IO3)n形式,其中碘酸根为-1价(类似于氯酸根),碘酸根中I为+5价,所以前面的I的化合价为+3价,将选项中的化学式进行变形,进行解答;
D.把杂质转化为沉淀或气体除去,除钙离子用碳酸根,除镁离子用氢氧根,除Fe3+用氢氧根,除硫酸根用钡离子.要注意除杂质的顺序,后加的试剂最好能把前面先加是过量试剂除掉.
解答 解:A.同位素是质子数相同,中子数不同的同种元素的不同原子,原子最外层电子数相同,化学性质相同,HDO与H2O化学性质相同,故A正确;
B.海水中含有镁离子,先将海水蒸发、浓缩得到含有镁离子的溶液,再向溶液中加入沉淀剂将Mg 2+转化为Mg(OH)2,加入的沉淀剂应该具有碱性且价格较廉价、来源丰富,贝壳中含有CaCO3且来源丰富,煅烧贝壳得到CaO,将CaO溶于水得到Ca(OH)2,所以加入的沉淀剂是Ca(OH)2,将镁离子转化为Mg(OH)2;将Mg(OH)2溶于稀盐酸得到MgCl2,将MgCl2在HCl氛围中加热得到MgCl2固体,电解熔融MgCl2得到Mg,MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑,故B正确;
C.因碘酸碘的化学式一定为Im(IO3)n形式,其中碘酸根为-1价(类似于氯酸根),碘酸根中I的化合价为+5价,所以前面的I的化合价为+3价,所以碘酸碘的化学式为:I(IO3)3,即 I4O9,故C正确;
D.除去粗盐中的可溶性杂质:Mg2+、Ca2+、Fe3+、SO42-时,可以加入过量NaOH(去除镁离子和铁离子):Mg2++2OH-=Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓,加入过量BaCl2(去除硫酸根离子):SO42-+Ba2+=BaSO4↓;加入过量Na2CO3(去除钙离子的多余的钡离子):Ca2++CO32-=CaCO3,碳酸钠必须加在氯化钡之后,氢氧化钠和氯化钡可以颠倒加入的顺序;然后调节溶液的pH等于7后蒸发即可,选项中过量的氯化钡不能除去,故D错误;
故选D.
点评 本题主要考查海水中提取镁的过程,粗盐提纯的实验方法应用,解题应抓住题目信息,知道每一步发生的反应及操作方法,再结合物质的性质进行解答,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题

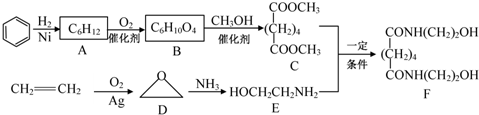
| A. | 化合物X、Y、Z中均有一个手性碳原子 | |
| B. | ①、②、③的反应类型依次为加成反应、还原反应和取代反应 | |
| C. | 由化合物Z一步制备化合物Y的转化条件是:NaOH醇溶液,加热 | |
| D. | 化合物Y先经酸性高锰酸钾溶液氧化,再与乙醇在浓硫酸催化下酯化可制得化合物X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气 | B. | 甲烷 | C. | 乙醇 | D. | 木炭 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若降低温度,可以加快反应速率 | |
| B. | 在上述条件下,SO2能完全转化为SO3 | |
| C. | 反应达平衡时,SO2和SO3的浓度一定相等 | |
| D. | 反应达平衡时,正反应速率和逆反应速率一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
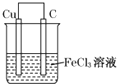
| A. | 将电能转换成化学能 | |
| B. | 碳棒上发生氧化反应 | |
| C. | 溶液中Cl-向铜棒一极移动 | |
| D. | 发生的总反应为:3Cu+2Fe3+═2Fe+3Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲酸甲酯的结构简式:C2H4O2 | B. | H2O2的电子式: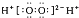 | ||
| C. | 中子数为10 的氧原子:188O | D. | 对-硝基甲苯的结构简式: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com