
 CH4是一种清洁、高效、具有优良的环保性能的燃料,1mol CH4完全燃烧生成稳定的产物.反应热为890.3KJ?mol-1.它可以作为燃料电池的燃料.
CH4是一种清洁、高效、具有优良的环保性能的燃料,1mol CH4完全燃烧生成稳定的产物.反应热为890.3KJ?mol-1.它可以作为燃料电池的燃料.| 2.8L |
| 22.4L/mol |


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
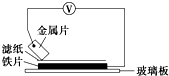 将洁净的金属片A、B、C、D分别放置在浸有盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下表所示:
将洁净的金属片A、B、C、D分别放置在浸有盐溶液的滤纸上面并压紧(如图所示).在每次实验时,记录电压指针的移动方向和电压表的读数如下表所示:| 金属 | 电子流动方向 | 电压/V |
| A | A→Fe | +0.76 |
| B | Fe→B | -0.18 |
| C | C→Fe | +1.32 |
| D | D→Fe | +0.28 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 ,单体为2-甲基-1,3-丁二烯(
,单体为2-甲基-1,3-丁二烯(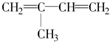 ),该加聚反应的化学方程式为:
),该加聚反应的化学方程式为:
 为单体生产氯丁橡胶,试写出该反应的化学方程式:
为单体生产氯丁橡胶,试写出该反应的化学方程式: )按物质的量之比为1:1加聚,可生产丁苯橡胶,试写出丁苯橡胶的结构简式:
)按物质的量之比为1:1加聚,可生产丁苯橡胶,试写出丁苯橡胶的结构简式: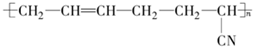 ,形成该橡胶的单体为:
,形成该橡胶的单体为:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④⑤ | B、②③④ |
| C、②③⑤ | D、只有①⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com