
| A�� | ${\;}_{27}^{60}$Coԭ�Ӻ��ں���60������ | |
| B�� | Co-59��Co-60��������ͬ�����߿ɻ���Ϊͬλ�� | |
| C�� | ${\;}_{27}^{59}$Coԭ�Ӻ��ں���22������ | |
| D�� | ${\;}_{27}^{60}$Coԭ�ӵ�����������Ϊ27 |
���� ������ͬ����������ͬ��������ͬһԪ�صIJ�ͬ���ػ�Ϊͬλ��ͬλ�أ�Ԫ�ط��ŵ����Ͻ����ִ���������A�����½����ִ���������Z��������N=������A-������Z��
��� �⣺A��${\;}_{27}^{60}$Co ԭ�Ӻ��ں���27�����ӣ���A����
B��Co-59��Co-60��������ͬ����������ͬ����������Ϊͬλ�أ���B��ȷ��
C��${\;}_{27}^{59}$Co ԭ�Ӻ��ں���59-27=32�����ӣ���C����
D��${\;}_{27}^{60}$Coԭ�ӵĺ������������Ϊ27����D����
��ѡ��B��
���� ���⿼��ͬλ�صĸ���ѶȲ���ע��ͬλ�ظ���������Լ�ԭ�������������������ı�����


 ���ѵ����Ԫ��ĩ���100��ϵ�д�
���ѵ����Ԫ��ĩ���100��ϵ�д� ��˼άС�ھ�100����ҵ��ϵ�д�
��˼άС�ھ�100����ҵ��ϵ�д� ��ʦָ��һ��ͨϵ�д�
��ʦָ��һ��ͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 SO2�Ĵ������ǹ�ҵ����������Ĺؼ����裮
SO2�Ĵ������ǹ�ҵ����������Ĺؼ����裮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������XԪ����2�� | |
| B�� | Y������������ˮ���ﲻ������ǿ�� | |
| C�� | Y���⻯���п��ܴ������Ӽ� | |
| D�� | Y�ĵ����ڳ����¿��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��NaH����ˮ���õ���ˮ��Һ�ܵ��磬�ɴ˿�˵��NaH�����ӻ����� | |
| B�� | Fe��OH��3�����Fe��OH��3�������������ʲ�ͬ����ѧ���ʻ�����ͬ | |
| C�� | CO2��SO2��SiO2��NO2�ȶ������������Na2O��MgO��A2lO3�ȶ��Ǽ��������� | |
| D�� | MnO2���н�ǿ�����ԣ�����ΪH2O2�ֽⷴӦ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH4+�ĵ�����Ϊ10 | B�� | H218O�ķ�����Ϊ18 | ||
| C�� | Be���������1������ | D�� | H-�ĵ��Ӳ�����2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 2mol C | |
| B�� | 2mol A��1mol B��1mol He�����μӷ�Ӧ�� | |
| C�� | 1mol B��1mol C | |
| D�� | 2mol A��3mol B��3mol C |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ʳ�� | B�� | �����Ǽ���ʳ�� | C�� | ����������ʳ�� | D�� | �����Ǽ���ʳ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
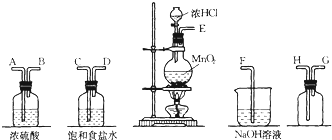
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com