
 2SO3(g);已知反应过程中某一时刻,SO2、O2、SO3分别是0.2mol/L、0.1mol/L、0.2mol/L,当反应达到平衡时,可能存在的数据是
2SO3(g);已知反应过程中某一时刻,SO2、O2、SO3分别是0.2mol/L、0.1mol/L、0.2mol/L,当反应达到平衡时,可能存在的数据是 | A.SO2为0.4mol/L,O2为0.2mol/L | B.SO3(g)为0.4mol/L |
| C.SO2、SO3(g)均为0.15mol/L | D.SO2为0.25mol/L |
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源:不详 题型:填空题
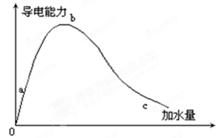
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.生成1mol乙酸乙酯的同时,也生成1mol乙酸 |
| B.乙酸、乙醇、乙酸乙酯的浓度相同 |
| C.当乙酸断开1mol碳氧单键的同时,乙醇也断开了1mol氢氧键 |
| D.当乙酸断开1mol氢氧键的同时,乙醇也断开了1mol碳氧单键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3(g) ΔH ="-98.3" kJ·mol-1。
2SO3(g) ΔH ="-98.3" kJ·mol-1。| 容 器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2 mol SO2、1 mol O2 | 2 mol SO3 | m mol SO2、n mol O2、 p mol SO3 |
| c(SO3) /mol·L-1 | 1.4 | 1.4 | 1.4 |
| 能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| SO2或SO3的转化率 | α1 | α2 | 12.5% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.凡是焓变小于零的反应都能自发进行 |
| B.凡是熵变小于零的化学反应都能自发进行 |
| C.凡是焓变小于零,熵变大于零的化学变化都能自发进行 |
| D.CaCO3在高温下的分解反应不属于自发过程 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NO2 (g)在下列过程中发生的变化描述正确的是
2NO2 (g)在下列过程中发生的变化描述正确的是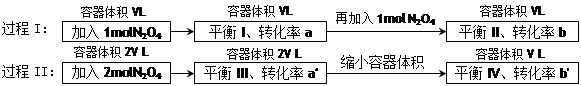
| A.a' < b'、a > b | B.在平衡I向平衡II过渡的过程中,v(逆) < v(正) |
| C.a' > a、b' < b | D.平衡II与平衡IV中N2O4的质量分数相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
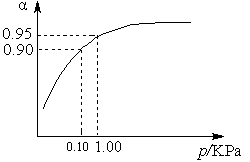
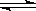 H2O(g)。我们也可以用平衡移动原理来解释这一变化中的一些问题,如:H2O
H2O(g)。我们也可以用平衡移动原理来解释这一变化中的一些问题,如:H2O 的汽化是吸热过程,所以温度升高,平衡向生成更多的H2O(g)的方向移动。请回答下面两个问题:
的汽化是吸热过程,所以温度升高,平衡向生成更多的H2O(g)的方向移动。请回答下面两个问题: 低)。高压锅中水的沸点比普通锅中水的沸点 (填高或低)。
低)。高压锅中水的沸点比普通锅中水的沸点 (填高或低)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 cC(g)(
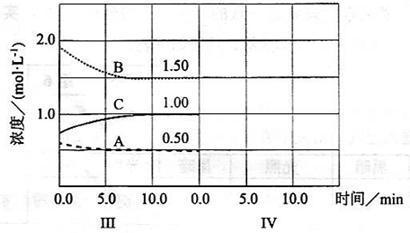
cC(g)(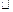 H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
H<0)在等容条件下进行。改变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示: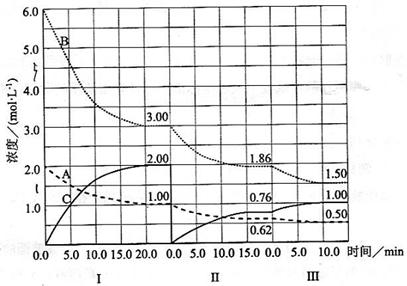
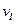 (A)、
(A)、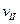 (A)、
(A)、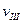 (A)从大到小排列次序为 ;
(A)从大到小排列次序为 ;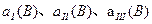 中最小的是 ,其值是 ;
中最小的是 ,其值是 ;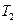 )和第III阶段反应速度(
)和第III阶段反应速度( )的高低:
)的高低: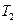

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com