工业上由FeS
2制H
2SO
4的转化关系如下:

填写下列空白:
(1)吸收塔中发生反应的化学方程式为
SO3+H2O=H2SO4
SO3+H2O=H2SO4
.
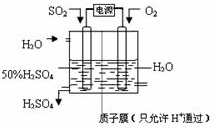
(2)接触室内发生的反应为:SO
2(g)+
O
2(g)
SO
3(g)△H=a kJ?mol
-1 下表为不同温度(T)下该反应的化学平衡常数(K):
| T/K |
673 |
723 |
823 |
923 |
| K |
423 |
37.4 |
20.5 |
4.68 |
①根据上表数据及化学平衡理论,上述反应中a
<
<
0(填“>”或“<”).
②K值越大,表明反应达到平衡时
C
C
(填标号).
A.SO
2的转化率一定越高 B.SO
3的产量一定越大
C.正反应进行得越完全 D.化学反应速率越大
(3)考虑综合经济效益,当炉渣含铁量大于45%时,可用于制硫酸亚铁等.下列利用炉渣里的Fe
2O
3制FeSO
4的方案中,最能体现绿色化学理念的方案是
B
B
(填标号)
A.Fe
2O
3Fe
FeSO
4B.Fe
2O
3Fe
2(SO
4)
3FeSO
C.Fe
2O
3Fe
FeSO
4D.Fe
2O
3Fe
FeSO
4(4)为实现绿色环保、节能减排和废物利用等目的,某硫酸厂用碳酸钙作吸收剂与水配成浆液,洗涤尾气(SO
2的体积分数为0.200%)并吸收SO
2,得到石膏(CaSO
4?2H
2O).求:22.4m
3(标准状况下)的尾气可制得石膏多少千克?(设二氧化硫的利用率为80.0%)




 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案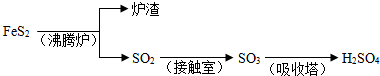

 O2(g)
O2(g) SO3(g)△H=a kJ?mol-1 下表为不同温度(T)下该反应的化学平衡常数(K):
SO3(g)△H=a kJ?mol-1 下表为不同温度(T)下该反应的化学平衡常数(K):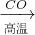 Fe
Fe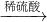 FeSO4
FeSO4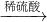 Fe2(SO4)3
Fe2(SO4)3 FeSO
FeSO 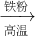 Fe
Fe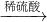 FeSO4
FeSO4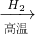 Fe
Fe FeSO4
FeSO4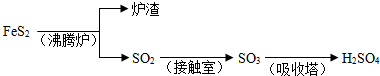

 O2(g)
O2(g)  SO3(g)△H=a kJ?mol-1
SO3(g)△H=a kJ?mol-1 Fe
Fe FeSO4;B.Fe2O3
FeSO4;B.Fe2O3 Fe2(SO4)3
Fe2(SO4)3 FeSO4;C.Fe2O3
FeSO4;C.Fe2O3 Fe
Fe FeSO4
FeSO4