
| A. | 5.6 g铁与足量Cl2充分反应,转移电子数为0.2×6.02×1023 | |
| B. | 由PbO2+4HCl(浓)═PbCl2+Cl2↑+2H2O可确定氧化性:PbO2>Cl2 | |
| C. | 2Na2O2(s)+2CO2(g)═2Na2CO3(s)+O2(g)在常温下能自发进行,则该反应的△H>0 | |
| D. | 常温下,用蒸馏水不断稀释0.1 mol•L-1醋酸,溶液中c(H+)/c(CH3COOH)的值减小 |
分析 A.氯气具有强氧化性,与变价金属反应生成高价态的氯化物,铁与足量氯气反应生成氯化铁;
B.自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
C.根据△G=△H-T•△S<0自发判断;
D.醋酸为弱酸,稀释过程中醋酸的电离程度增大,溶液中氢离子、醋酸根离子的物质的量增大,醋酸的物质的量减小,再结合溶液体积相同分析.
解答 解:A.5.6g铁为0.1mol,与足量氯气充分反应生成氯化铁,转移的电子数为0.3NA,即转移电子数为0.3×6.02×1023,故A错误;
B.PbO2+4HCl═PbCl2+Cl2↑+2H2O 中Pb元素化合价由+4价变为+2价、Cl元素化合价由-1价变为0价,所以 PbO2是氧化剂、Cl2是氧化产物,氧化性PbO2>Cl2,故B正确;
C.2Na2O2(s)+2CO2(g)═2Na2CO3(s)+O2(g),气体体积减小混乱度减小,△S<0,在常温下能自发进行,△G=△H-T•△S<0,则该反应的△H<0,故C错误;
D.稀释过程中氢离子的物质的量增大、醋酸的物质的量减小,由于在同一溶液中,溶液体积相同,则溶液中c(H+)/c(CH3COOH)的值增大,故D错误;
故选B.
点评 本题考查了氯气的性质、氧化性的比较、反应进行的方向判断、以及弱电解质的电离,掌握相关的知识是解答关键,试题培养了学生的灵活应用基础知识的能力,题目难度中等.


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥ | B. | ①④⑤ | C. | ②③⑥ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的能量一定低于M的,Y的能量一定低于N的 | |
| B. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| C. | 破坏反应物中的化学键所吸收的能量大于形成生成物中化学键所放出的能量 | |
| D. | 反应物X和Y的总能量一定大于生成物M和N的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu+HNO3(稀) | B. | N2+O2 | C. | NH4Cl+O2 | D. | NO2+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
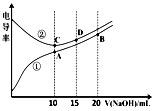
| A. | 曲线①代表滴定CH3COOH溶液的曲线 | |
| B. | A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.05mol•L-1 | |
| C. | 在相同温度下,A、B、C三点溶液中水电离的c(H+):B<A=C | |
| D. | B点溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应①使用催化剂,能降低该反应的活化能 | |
| B. | 反应②为吸热反应 | |
| C. | 反应③将化学能转化为光能 | |
| D. | 反应CO(g)+H2O(g)═CO2(g)+H2(g);△H=-82.4 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Mg、Al的金属性依次减弱 | B. | H2S、H2O、HF的稳定性依次减弱 | ||
| C. | Cl-、Br-、I- 还原性依次增强 | D. | Na、K、Rb的原子半径依次增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子半径X>Y>Z | |
| B. | 离子半径Ym->Xn+>Zm+ | |
| C. | 三种元素最高价氧化物对应水化物碱性依次减弱,酸性依次增强的顺序是X,Z,Y | |
| D. | Y在自然界中没有游离态,可形成原子晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com