
| A. | CO2通入澄清的石灰水中反应的产物 $\frac{n(C{O}_{2})}{n[Ca(OH)_{2}]}$ $\frac{n(C{O}_{2})}{n[Ca(OH)_{2}]}$ | |
| B. | Fe在Cl2中的燃烧产物: $\frac{n(C{l}_{2})}{n(Fe)}$ $\frac{n(C{l}_{2})}{n(Fe)}$ | |
| C. | AlCl3溶液中滴加NaOH后铝的存在形式: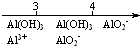 $\frac{n(NaOH)}{n(AlC{l}_{3})}$ $\frac{n(NaOH)}{n(AlC{l}_{3})}$ | |
| D. | 氨水与SO2反应后溶液中的铵盐: $\frac{n(N{H}_{3}{H}_{2}O)}{n(S{O}_{2})}$11 $\frac{n(N{H}_{3}{H}_{2}O)}{n(S{O}_{2})}$11 |
分析 A.根据发生的反应Ca(OH)2+CO2═CaCO3↓+H2O;CaCO3+CO2+H2O═Ca(HCO3)2分析;
B.Fe在Cl2中燃烧的产物与Fe和Cl2的用量无关,其产物只有FeCl3;
C.根据可能发生的反应Al3++3OH-=Al(OH)3↓,Al3++4OH-=AlO2-+2H2O分析;
D.根据可能发生的反应有:NH3•H2O+SO2=NH4HSO3,2NH3•H2O+SO2=(NH4)2SO3+H2O进行分析.
解答 解:A.反应的化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O;CaCO3+CO2+H2O═Ca(HCO3)2,CO2与Ca(OH)2的物质的量之比为1:1时,恰好反应生成CaCO3,即CO2与Ca(OH)2的物质的量之比为≤1时反应得到CaCO3,CO2与Ca(OH)2的物质的量之比为2:1时,恰好反应生成Ca(HCO3)2,即CO2与Ca(OH)2的物质的量之比为≥2时反应得到Ca(HCO3)2,故A错误;
B.Fe在Cl2中燃烧只有一种产物FeCl3,产物与$\frac{n(C{l}_{2})}{n(Fe)}$无关,故B错误;
C.Al3++3OH-=Al(OH)3↓,Al3++4OH-=AlO2-+2H2O,$\frac{n(NaOH)}{n(AlC{l}_{3})}$<3,铝元素以Al3+和Al(OH)3形式存在; $\frac{n(NaOH)}{n(AlC{l}_{3})}$=3,则以Al(OH)3形式存在;3<$\frac{n(NaOH)}{n(AlC{l}_{3})}$<4以 AlO2-和Al(OH)3形式存在; $\frac{n(NaOH)}{n(AlC{l}_{3})}$≥4只以 AlO2-形式存在,故C正确;
D.NH3•H2O+SO2=NH4HSO3,2NH3•H2O+SO2=(NH4)2SO3+H2O,$\frac{n(N{H}_{3}{H}_{2}O)}{n(S{O}_{2})}$≤1,生成NH4HSO3;1<$\frac{n(N{H}_{3}{H}_{2}O)}{n(S{O}_{2})}$<2,产物为NH4HSO3与(NH4)2SO3混合物;$\frac{n(N{H}_{3}{H}_{2}O)}{n(S{O}_{2})}$≥2,只生成(NH4)2SO3,故D正确.
故选AB.
点评 本题是近年以来出现的一道很少出现的试题题型题,是一道新情景试题,具有很强的综合性,也具有极强的迷惑性,各选项具有很强的干扰性,是一道好题!很容易选错答案.主要考查学生对元素化合物知识的掌握情况.注意Fe在Cl2中燃烧的产物与Fe和Cl2的用量无关,其产物只有FeCl3.


科目:高中化学 来源: 题型:选择题
| A. | 苯分子的核磁共振图表明分子中只存在一种氢原子 | |
| B. | 邻二甲苯没有同分异构体 | |
| C. | 间二甲苯没有同分异构体 | |
| D. | 对二甲苯没有同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 | 4.7 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 乙醇脱水反应在不同温度条件下得到的产物组成不同.表是常压、某催化剂存在条件下,分别以等量乙醇在不同温度下进行脱水实验获得的数据,每次实验反应时间均相同.
乙醇脱水反应在不同温度条件下得到的产物组成不同.表是常压、某催化剂存在条件下,分别以等量乙醇在不同温度下进行脱水实验获得的数据,每次实验反应时间均相同.| 温度(℃) | 乙醇转化率(%) | 有机产物含量(体积分数) | |
| 乙烯(%) | 乙醚(%) | ||
| 125 | 20 | 8.7 | 90.2 |
| 150 | 68 | 16.7 | 82.2 |
| 175 | 88 | 32.3 | 66.8 |
| 200 | 90 | 86.9 | 12.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 .
. (其中任一种).
(其中任一种).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com