
【题目】四氯化锡常用作媒染剂、有机合成中的催化剂,已知SnCl4易水解,溶点为﹣33℃、沸电为114℃.某研究性学习小组设计如图装置(部分夹持装置及加热仪器省略)制备SnCl4 . 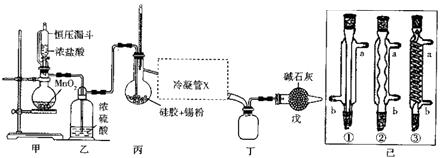
(1)装置甲中反应的离子方程式为 . 整个制备装置中有一处不足,改进的方法是
(2)利用改进后的装置进行实验(下同)时甲、丙均需加热,首先加热的是处的烧瓶,冷凝管x是已中的一种,该仪器的编号是 , 装置戊的用途是 .
(3)实验过程中装置甲中除观察到固体溶解外,还可观察到的明显变化是 .
(4)该小组的甲同学提出,可利用标准NaOH溶液滴定甲中剩余溶液的方法测定出盐酸与MnO2反应的最低浓度.
①滴定时所用指示剂最好是[假设开始出现Mn( OH)2 , 沉淀时的pH约为6,8].
②假设实验时从甲中准确取出V2mL剰余溶液并稀释到V3 mL,然后用0.100 0molL﹣1的 NaOH溶液进行滴定,滴定终点时消耗掉V1mL NaOH溶液,则盐酸与MnO2反应时最低浓度应大于 .
【答案】
(1)MnO2+4H++2Cl﹣ ![]() Mn2++2H2O+Cl2↑;甲与乙之间连一个盛有饱和食盐水的洗气瓶
Mn2++2H2O+Cl2↑;甲与乙之间连一个盛有饱和食盐水的洗气瓶
(2)甲;①;防止空气中水份进入丁装置,同时可以吸收氯气尾气
(3)有黄绿色气体生成
(4)甲基橙;![]() mol/L
mol/L
【解析】解:根据实验装置图可知,甲装置用MnO2和浓盐酸在加热条件下制取氯气,发生的反应为MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,乙装置用浓硫酸干燥氯气,丙装置用锡与氯气反应生成SnCl4 , 为了便于生成 的液态SnCl4顺利流下,应用直形冷凝管冷却,SnCl4易水解,为防止空气中水份进入丁与生成的SnCl4反应,丁后面连接一个戊装置,同时可以吸收氯气尾气,在制氯气的实验中,浓盐酸具有挥发性,加热促进挥发,所以生成的氯气中含有HCl,为防止Sn与HCl反应,在甲与乙之间还应再加一个除氯化氢的装置,即连一个盛有饱和食盐水的洗气瓶,利用标准NaOH溶液滴定甲中剩余溶液中的盐酸浓度,要防止锰离子出现沉淀,所以滴定终点的PH值要小于6.8,所以要用甲基橙做指示剂,根据氢氧化钠的物质的量可计算出V2mL剰余溶液中氯化氢的物质的量,进而可计算出此时溶液中氯化氢的物质的量浓度,(1)装置甲中用MnO2和浓盐酸在加热条件下制取氯气,反应的离子方程式为 MnO2+4H++2Cl﹣
MnCl2+Cl2↑+2H2O,乙装置用浓硫酸干燥氯气,丙装置用锡与氯气反应生成SnCl4 , 为了便于生成 的液态SnCl4顺利流下,应用直形冷凝管冷却,SnCl4易水解,为防止空气中水份进入丁与生成的SnCl4反应,丁后面连接一个戊装置,同时可以吸收氯气尾气,在制氯气的实验中,浓盐酸具有挥发性,加热促进挥发,所以生成的氯气中含有HCl,为防止Sn与HCl反应,在甲与乙之间还应再加一个除氯化氢的装置,即连一个盛有饱和食盐水的洗气瓶,利用标准NaOH溶液滴定甲中剩余溶液中的盐酸浓度,要防止锰离子出现沉淀,所以滴定终点的PH值要小于6.8,所以要用甲基橙做指示剂,根据氢氧化钠的物质的量可计算出V2mL剰余溶液中氯化氢的物质的量,进而可计算出此时溶液中氯化氢的物质的量浓度,(1)装置甲中用MnO2和浓盐酸在加热条件下制取氯气,反应的离子方程式为 MnO2+4H++2Cl﹣ ![]() Mn2++2H2O+Cl2↑,根据上面的分析可知,整个制备装置中有一处不足,改进的方法是甲与乙之间连一个盛有饱和食盐水的洗气瓶,所以答案是:MnO2+4H++2Cl﹣
Mn2++2H2O+Cl2↑,根据上面的分析可知,整个制备装置中有一处不足,改进的方法是甲与乙之间连一个盛有饱和食盐水的洗气瓶,所以答案是:MnO2+4H++2Cl﹣ ![]() Mn2++2H2O+Cl2↑;甲与乙之间连一个盛有饱和食盐水的洗气瓶;(2)由于SnCl4易水解,在实验过程中要将装置中的空气全部排尽,所以在实验时,首先加热的是甲处的烧瓶,根据上面的分析可知,冷凝管x是直形冷凝管,该仪器的编号是①,装置戊的用途是 防止空气中水份进入丁装置,同时可以吸收氯气尾气,
Mn2++2H2O+Cl2↑;甲与乙之间连一个盛有饱和食盐水的洗气瓶;(2)由于SnCl4易水解,在实验过程中要将装置中的空气全部排尽,所以在实验时,首先加热的是甲处的烧瓶,根据上面的分析可知,冷凝管x是直形冷凝管,该仪器的编号是①,装置戊的用途是 防止空气中水份进入丁装置,同时可以吸收氯气尾气,
所以答案是:甲;①;防止空气中水份进入丁装置,同时可以吸收氯气尾气;(3)实验过程中装置甲中除观察到固体溶解外,还可观察到的明显变化是有黄绿色气体生成,
所以答案是:有黄绿色气体生成;(4)①利用标准NaOH溶液滴定甲中剩余溶液中的盐酸浓度,要防止锰离子出现沉淀,所以滴定终点的PH值要小于6.8,所以要用甲基橙做指示剂,
所以答案是:甲基橙;②根据题意,NaOH的物质的量为0.100 0molL﹣1×V1mL,所以V2mL剰余溶液中氯化氢的物质的量为0.100 0molL﹣1×V1mL,则盐酸浓度为 ![]() =
= ![]() mol/L,所以盐酸与MnO2反应时最低浓度应大于
mol/L,所以盐酸与MnO2反应时最低浓度应大于 ![]() mol/L,
mol/L,
所以答案是: ![]() mol/L.
mol/L.


科目:高中化学 来源: 题型:
【题目】常温下,0.2molL﹣1的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法不正确的是( ) 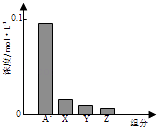
A.HA为弱酸
B.该混合液pH>7
C.图中X表示HA,Y表示OH﹣ , Z表示H+
D.该混合溶液中:c(A﹣)+c(Y)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素X,Y的核电荷数分别为a和b,它们的离子Xn+的Ym-的核外电子排布完全相同,则下列关系中正确的是 ( )
A. a+m=b-nB. a+b=m+nC. a-m=b+nD. a+m=b-n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含Fe2(SO4)3、CuCl2、H2SO4的混合溶液中投入足量的Fe粉,充分反应后,剩余的固体物质经干燥,称得其质量比加入的铁粉质量减轻16g,此时溶液中c(Fe2+)是原混合液中c(Cu2+)的3倍(反应前后体积没有变化),溶液中c(SO42﹣)与c(Cl﹣)之比是( )
A.1:2
B.2:1
C.1:3
D.1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关葡萄糖的说法错误的是( )
A.葡萄糖的分子式为C6H12O6
B.葡萄糖能发生银镜反应
C.葡萄糖是人体重要的能量来源
D.葡萄糖属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SO2组成,由蛇纹石制取碱式碳酸镁的实验步骤如图1: 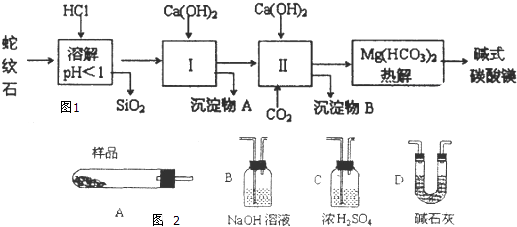
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是 .
(2)进行I操作时,控制溶液的pH=7.8(有关氢氧化物沉淀的pH见下表),Ca(OH)2不能过量,若Ca(OH)2过量可能会导致溶解,产生沉淀.
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 1.9 | 3.3 | 9.4 |
沉淀完全时PH | 3.2 | 5.4 | 12.4 |
(3)从沉淀混合物A中提取红色氧化物作为颜料,先向沉淀物A中加入(填所加物质的化学式),然后、、灼烧(填实验操作名称).灼烧操作需在中进行(填写仪器名称),上述实验中,可以循环利用的物质是(填化学式).
(4)现设计实验,确定产品aMgCO3bMg(OH)2cH2O中a、b、c的值,请写出下列实验步骤中所需要测定的项目(可用试剂:浓硫酸、碱石灰、氢氧化钠溶液、澄清石灰水):①样品称量,②高温分解,③测出水蒸气的质量,④ , ⑤称量MgO的质量.
(5)从下列仪器图2中(装有必要的试剂)中选择完成上述实验所必需的仪器,连接一套装置(选择仪器代号,可重复使用,用“A→B→…→”表示)
(6)18.2g产品完全分解后.产生6.6gCO2和8.0gMgO,由此可知,产品的化学式中 a= , b= , c= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖的分子式为C6H12O6 , 下列关于葡萄糖的说法错误的是( )
A.葡萄糖由碳、氢、氧三种元素组成
B.葡萄糖分子中氢、氧原子个数比为2∶1
C.葡萄糖的相对分子质量为188
D.葡萄糖在人体内氧化可提供能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.糖类是指含C、H、O三种元素的有机物
B.糖类物质的组成都符合通式Cm(H2O)n
C.动植物的生命活动都需要糖
D.分子中含一个官能团的糖称为单糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以一种工业废渣(主要成分为MgCO3、Mg2SiO4和少量Fe、Al的氧化物)为原料制备MgCO33H2O.实验过程如图1: 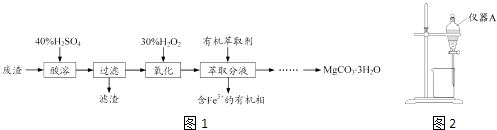
(1)酸溶过程中主要反应的热化学方程式为
MgCO3(s)+2H+(aq)═Mg2+(aq)+CO2(g)+H2O(l)△H=﹣50.4kJmol﹣1
Mg2SiO4(s)+4H+(aq)═2Mg2+(aq)+H2SiO3(s)+H2O(l)△H=﹣225.4kJmol﹣1
酸溶需加热的目的是_;所加H2SO4不宜过量太多的原因是 .
(2)加入H2O2氧化时发生发应的离子方程式为
(3)用图2所示的实验装置进行萃取分液,以除去溶液中的Fe3+ .
①实验装置图中仪器A的名称为 .
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有水溶液的仪器A中加入一定量的有机萃取剂,、静置、分液,并重复多次.
(4)请补充完整由萃取后得到的水溶液制备MgCO33H2O的实验方案:边搅拌边向溶液中滴加氨水, , 过滤、用水洗涤固体2~3次,在50℃下干燥,得到MgCO33H2O.
已知该溶液中pH=8.5时Mg(OH)2开始沉淀;pH=5.0时Al(OH)3沉淀完全].
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com