
| A. | 高铁酸钠中铁显+6价 | |
| B. | 湿法中FeO42-是氧化产物 | |
| C. | 干法中每生成1 molNa2FeO4转移4mol电子 | |
| D. | Na2FeO4可氧化水中的H2S、NH3,生成的Fe(OH)3胶体还能吸附悬浮杂质 |
分析 A、根据化合物中正负化合价的代数和为0进行解答;
B、氧化产物是还原剂被氧化得到的产物;
C、化合价升高数=化合价降低数=转移电子数;
D、依据高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强、无二次污染的绿色水处理剂分析.
解答 解:A、根据高铁酸钾的化学式(K2FeO4)可知,设铁元素的化合价为x,则+1×2+x+(-2)×4=0,解得x=+6,故A正确;
B、湿法中Fe(OH)3被氧化生成的FeO42-是氧化产物,故B正确;
C、反应2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑中,铁元素化合价升高,每生成2molNa2FeO4,转移电子总数=化合价升高总数=化合价降低总数=8mol,所以每生成1molNa2FeO4共转移4mol电子,同时1molNa2O2变化生成1molO2,化合价升高,转移电子物质的量为2mol,所以共转移电子10mol,故C错误;
D、K2FeO4具有氧化性所以能杀菌,H2S、NH3具有还原性被氧化,高铁酸钾与水反应时生成的Fe(OH)3(胶体)具有净水作用,故D正确;
故选C.
点评 本题考查了氧化还原反应的化合价变化判断,概念分析和电子转移数计算,熟练掌握氧化还原反应的特征是化合价变化是关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | NH3溶于水后显碱性,在FeCl3饱和溶液中通入足量NH3可制取Fe(OH)3胶体 | |
| B. | NaHCO3能与碱反应,食品工业上用作焙制糕点的膨松剂 | |
| C. | Mg(OH)2分解吸热且生成高熔点固体,可用作阻燃剂 | |
| D. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 电极材料 | Cu、Zn | Cu、Ag | Fe、Zn | Cu、C |
| 插入溶液 | FeCl3 | Fe(NO3) 2 | CuSO4 | Fe2(SO4)3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
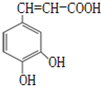
| A. | 分子式为C9H8O4 | |
| B. | 1mol咖啡酸最多能与4mol氢气发生加成反应 | |
| C. | 遇溴水,既能发生取代反应又能发生加成反应 | |
| D. | 能还原酸性KMnO4溶液,说明其分子中含有碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同种物质 | B. | 不同密度的核素 | ||
| C. | 同位素 | D. | 相同元素构成的不同单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 偏铝酸钡 Ba(AlO2)2 | B. | 明矾 KAl(SO4)2•12H2O | ||
| C. | 醋酸钙 (CH3COO)2Ca | D. | 亚硫酸氢钙 CaHSO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨的喷泉实验:圆底烧瓶 | B. | 实验室制氧气:试管 | ||
| C. | 中和滴定:锥形瓶 | D. | 中和滴定:滴定管 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

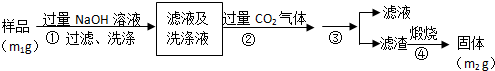
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度 | B. | 降低温度 | C. | 通入氦气 | D. | 加入催化剂 | ||||
| E. | 移出氧气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com