
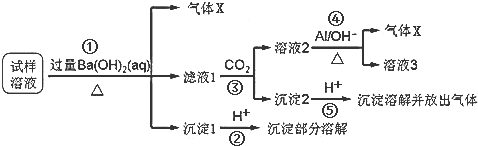
分析 试样溶液中加入过量Ba(OH)2并加热,生成的气体X,该气体X是NH3,则试样中含有NH4+;向滤液中通入CO2,得到溶液2、沉淀2,溶液2中加入Al,3NO3-+8Al+5OH-+2H2O$\stackrel{△}{→}$3NH3+8AlO2-,生成气体X,该气体是NH3,根据已知条件知,溶液2中含有NO3-,根据元素守恒知,原溶液中含有NO3-;滤液1中通入CO2,得到沉淀2,向沉淀2中加入酸,沉淀溶解并放出气体,说明沉淀2是碳酸钡等难溶性碳酸盐;沉淀1加入酸后,沉淀部分溶解,硫酸钡不溶于酸,说明原来溶液中含有SO42-,能和过量Ba(OH)2反应生成能溶于酸的沉淀,根据离子知,该沉淀为Mg(OH)2,所以溶液中含有Mg 2+,结合题给选项分析解答.
解答 解:试样溶液中加入过量Ba(OH)2并加热,生成的气体X,该气体X是NH3,则试样中含有NH4+;向滤液中通入CO2,得到溶液2、沉淀2,溶液2中加入Al,NO3-+A1+OH-+H2O→NH3↑+[Al(OH)4]-,生成气体X,该气体是NH3,根据已知条件知,溶液2中含有NO3-,根据元素守恒知,原溶液中含有NO3-;滤液1中通入CO2,得到沉淀2,向沉淀2中加入酸,沉淀溶解并放出气体,说明沉淀2是碳酸钡等难溶性碳酸盐;沉淀1加入酸后,沉淀部分溶解,硫酸钡不溶于酸,说明原来溶液中含有SO42-,能和过量Ba(OH)2反应生成能溶于酸的沉淀,根据离子知,该沉淀为Mg(OH)2,所以溶液中含有Mg 2+,
(1)试样溶液中加入过量Ba(OH)2并加热,生成的气体X是NH3;生成的沉淀1为Mg(OH)2、BaSO4;
故答案为:NH3;Mg(OH)2、BaSO4;
(2)滤液1中通入CO2,得到沉淀2,向沉淀2中加入酸,沉淀溶解并放出气体,离子方程式为BaCO3+2H+=Ba2++CO2↑+H2O,沉淀2是碳酸钡等难溶性碳酸盐,也有可能是试样中存在Al3+,在过量的Ba(OH)2中反应生成AlO2-,通入CO2后生成Al(OH)3沉淀,反应的离子方程式为:2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32-;
故答案为:BaCO3+2H+=Ba2++CO2↑+H2O;2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32-;
(3)第④步发生反应为3NO3-+8Al+5OH-+2H2O$\stackrel{△}{→}$3NH3+8AlO2-,每当生成3mol氨气,转移24mol电子,每产生5.6L标准状况下的气体NH3即0.25mol,转移电子为2mol,
故答案为:2mol.
点评 本题考查了物质的推断,明确物质的性质及特殊反应现象是解本题关键,根据物质的溶解性、物质的性质及题给信息来分析解答,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 将水加热到100℃时,水的pH=6 | B. | 向水中滴加少量稀H2SO4 | ||
| C. | 向水中加入少量NaHCO3 | D. | 向水中加入少量胆矾晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室中少量金属钠通常保存在煤油中 | |
| B. | 光线通过时,胶体可产生丁达尔效应 | |
| C. | 氧气、液氯是单质,氯水、氯化氢、纯碱是化合物. | |
| D. | “只要工夫深,铁杵磨成针”只涉及物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某校课外活动小组利用NO2与N2O4的反应来探究温度对化学平衡的影响.
某校课外活动小组利用NO2与N2O4的反应来探究温度对化学平衡的影响.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol 氧气中含有12.04×1023个氧原子,在标准状况下占有体积22.4 L | |
| B. | 1 mol臭氧和1.5 mol氧气含有相同的氧原子数 | |
| C. | 等体积、浓度均为1 mol•L-1的磷酸和盐酸,H3PO4和HCl含有的氢元素质量之比为1:1 | |
| D. | 等物质的量的干冰和葡萄糖(C6H12O6)中所含碳原子数之比为1:6,氧原子数之比为1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应:SO2(g)+NO2(g)?SO3(g)+NO(g) 达到平衡,正反应速率随时间变化如图所示.则正确的结论是( )
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应:SO2(g)+NO2(g)?SO3(g)+NO(g) 达到平衡,正反应速率随时间变化如图所示.则正确的结论是( )| A. | 逆反应速率:a点大于点c | |
| B. | 反应物浓度:a点小于点b | |
| C. | 反应在c点时SO2的转化率最大 | |
| D. | 反应物的总能量低于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当生成沉淀达到最大量时,消耗NaOH溶液的体积为150mL | |
| B. | 当金属全部溶解时收集到NO气体的体积为4.48L(标准状况下) | |
| C. | 参加反应的金属的总质量一定是9.9g | |
| D. | 当金属全部溶解时,参加反应的硝酸的物质的量一定是0.6mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com