
ЁОЬтФПЁПюмЃЈCoЃЉЪЧвЛжжживЊЕФеНТдН№ЪєЃЌюмМАЦфКЯН№ЙуЗКгІгУгкЕчЛњЁЂЛњаЕЁЂЛЏЙЄЁЂКНПеКЭКНЬьЕШСьгђЁЃюмдкЛЏКЯЮяжаЭЈГЃвд+2ЁЂ+3ЕФаЮЪНДцдкЁЃ
ЃЈ1ЃЉаДГіЛљЬЌCoдзгЕФКЫЭтЕчзгХХВМЪН___________________ЃЛ
ЃЈ2ЃЉCo2+ЁЂCo3+ЖМФмгыCN-аЮГЩХфЮЛЪ§ЮЊ6ЕФХфРызгЁЃCN-жаЬМдзгЕФдгЛЏЗНЪНЮЊ_____ЃЛ1mol HCNЗжзгжаІвМќЕФЪ§ФПЮЊ_________ЁЃ
ЃЈ3ЃЉCoЕФвЛжжбѕЛЏЮяЕФОЇАћШчЭМЫљЪОЃЈЦфжаКкЧђДњБэCoЃЉЃЌдђИУбѕЛЏЮяЕФЛЏбЇЪНЮЊ_______ЃЌдкИУОЇЬхжагывЛИібѕРызгЕШОрРыЧвзюНќЕФCoРызгЫљаЮГЩЕФПеМфЙЙаЭЮЊ___________ЁЃ
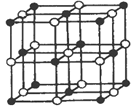
ЃЈ4ЃЉгУKCNДІРэКЌCo2+ЕФбЮШмвКЃЌгаКьЩЋЕФCo(CN)2ЮіГіЃЌНЋЫќШмгкЙ§СПЕФKCNШмвККѓЃЌПЩЩњГЩзЯЩЋЕФ[Co(CN)6]4-ЃЌИУХфРызгЪЧвЛжжЯрЕБЧПЕФЛЙдМСЃЌдкМгШШЪБФмгыЫЎЗДгІЩњГЩ[Co(CN)6]3-ЃЌаДГіИУЗДгІЕФРызгЗНГЬЪН__________________ЁЃ
ЁОД№АИЁП1s22s22p63s23p63d74s2 sp 2NA CoO е§АЫУцЬх 2[Co(CN)6]4- +2H2O=2[Co(CN)6]3-+H2Ёќ+2OH-
ЁОНтЮіЁП
ЃЈ1ЃЉCoЪЧ27КХдЊЫиЃЌКЫЭтЕчзгЪ§ЮЊ27ЃЌЦфКЫЭтЕчзгХХВМЪНЮЊ1s22s22p63s23p63d74s2ЁЃ
ЃЈ2ЃЉCN-жаЬМдзгЕФМлВуЕчзгЖдЪ§=1+![]() ЃН2ЁЂКЌга1ЖдЙТЕчзгЖдЃЌCдзгВЩШЁspдгЛЏЗНЪНЃЛHCNЕФНсЙЙЪНЮЊHЁЊCЁдNЃЌЕЅМќЮЊІвМќЃЌШ§МќжаКЌ1ИіІвМќКЭ2ИіІаМќЃЌдђ1ИіHCNЗжзгжаКЌга2ИіІвМќЃЌЙЪ1molHCNЗжзгжаІвМќЕФЪ§ФПЮЊ 2NAЁЃ
ЃН2ЁЂКЌга1ЖдЙТЕчзгЖдЃЌCдзгВЩШЁspдгЛЏЗНЪНЃЛHCNЕФНсЙЙЪНЮЊHЁЊCЁдNЃЌЕЅМќЮЊІвМќЃЌШ§МќжаКЌ1ИіІвМќКЭ2ИіІаМќЃЌдђ1ИіHCNЗжзгжаКЌга2ИіІвМќЃЌЙЪ1molHCNЗжзгжаІвМќЕФЪ§ФПЮЊ 2NAЁЃ
ЃЈ3ЃЉОЇАћжаCoдзгЪ§ФП=8ЁС![]() +6ЁС
+6ЁС![]() =4ЁЂOдзгЪ§ФП=1+12ЁС
=4ЁЂOдзгЪ§ФП=1+12ЁС![]() =4ЃЌЙЪЛЏбЇЪНЮЊCoOЃЛвдЬхаФЕФOдзгбаОПЃЌгыжЎЕШОрРыЧвзюНќЕФCoРызгЮЛгкУцаФЩЯЃЌCoРызгЫљаЮГЩЕФПеМфЙЙаЭЮЊе§АЫУцЬхЁЃ
=4ЃЌЙЪЛЏбЇЪНЮЊCoOЃЛвдЬхаФЕФOдзгбаОПЃЌгыжЎЕШОрРыЧвзюНќЕФCoРызгЮЛгкУцаФЩЯЃЌCoРызгЫљаЮГЩЕФПеМфЙЙаЭЮЊе§АЫУцЬхЁЃ
ЃЈ4ЃЉ[Co(CN)6]4-ОпгаЧПЛЙдадЃЌФмгыЫЎЗДгІЩњГЩ[Co(CN)6]3-гыЧтЦјЃЌИљОндзгЪиКугыЕчКЩЪиКуПЩжЊЛЙгаOH-ЩњГЩЃЌЗДгІРызгЗНГЬЪНЮЊ2[Co(CN)6]4-+2H2OЃН2[Co(CN)6]3-+H2Ёќ+2OH-ЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПввБНДпЛЏЭбЧтжЦБНввЯЉЗДгІЃК![]() +H2(g)ЁЃ
+H2(g)ЁЃ
ЙЄвЕЩЯЃЌЭЈГЃдкввБНеєЦјжаВєЛьЫЎеєЦј(дСЯЦјжаввБНКЭЫЎеєЦјЕФЮяжЪЕФСПжЎБШЮЊ1ЉU9)ЃЌПижЦЗДгІЮТЖШ600ЁцЃЌВЂБЃГжЬхЯЕзмбЙЮЊГЃбЙЕФЬѕМўЯТНјааЗДгІЁЃдкВЛЭЌЗДгІЮТЖШЯТЃЌввБНЕФЦНКтзЊЛЏТЪКЭФГДпЛЏМСзїгУЯТБНввЯЉЕФбЁдёад(жИГ§СЫH2вдЭтЕФВњЮяжаБНввЯЉЕФЮяжЪЕФСПЗжЪ§)ЪОвтЭМШчЭМЃК
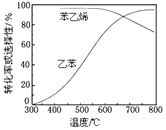
ЂйВєШыЫЎеєЦјФмЬсИпввБНЕФЦНКтзЊЛЏТЪЃЌНтЪЭЫЕУїИУЪТЪЕ___ЁЃ
ЂкПижЦЗДгІЮТЖШЮЊ600ЁцЕФРэгЩЪЧ___ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
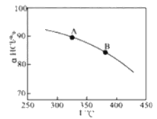
ЁОЬтФПЁПгУO2НЋHClзЊЛЏЮЊCl2ЃЌПЩЬсИпаЇвцЃЌМѕЩйЮлШОЃЌ
аТаЭRuO2ДпЛЏМСЖдЩЯЪіHClзЊЛЏЮЊCl2ЕФзмЗДгІОпгаИќКУЕФДпЛЏЛюадЃЌ
дкЩЯЪіЪЕбщжаШєбЙЫѕЬхЛ§ЪЙбЙЧПдіДѓЃЌЛГіЯргІaHClЁЊTЧњЯпЕФЪОвтЭМЃЌВЂМђвЊЫЕУїРэгЩ___ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПДѓЦјжаCO2КЌСПЕФдіМгЛсМгОчЮТЪваЇгІЃЌЮЊМѕЩйЦфХХЗХЃЌашНЋЙЄвЕЩњВњжаВњЩњЕФCO2ЗжРыГіРДНјааДЂДцКЭРћгУЁЃ
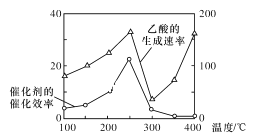
вдTiO2/Cu2Al2O4ЮЊДпЛЏМСЃЌПЩвдНЋCO2КЭCH4жБНгзЊЛЏЮЊввЫсЃЌЧыаДГіИУЗДгІЕФЛЏбЇЗНГЬЪНЃК____ЁЃдкВЛЭЌЮТЖШЯТДпЛЏМСЕФДпЛЏаЇТЪгыввЫсЕФЩњГЩЫйТЪЕФЙиЯЕШчЭМЫљЪОЁЃдкЮТЖШЮЊ____ЪБЃЌДпЛЏМСЕФЛюадзюКУЃЌаЇТЪзюИпЁЃЧыНтЪЭЭМжа250ЁЋ400ЁцЪБввЫсЩњГЩЫйТЪБфЛЏЕФдвђЃК250ЁЋ300ЁцЪБ___ЃЛ300ЁЋ400ЁцЪБ___ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаа№Ъіе§ШЗЕФЪЧЃЈ ЃЉ
A. ЗжзгЪНЮЊC4H8гаЛњЮязюЖрДцдк4ИіCЉCЕЅМќ
B. ![]() КЭ
КЭ![]() ОљЪЧЗМЯуЬўЃЌ
ОљЪЧЗМЯуЬўЃЌ![]() МШЪЧЗМЯуЬўгжЪЧЗМЯуЛЏКЯЮя
МШЪЧЗМЯуЬўгжЪЧЗМЯуЛЏКЯЮя
C. ![]() КЭ
КЭ![]() ЗжзгзщГЩЯрВювЛИіЉCH2ЉЃЌвђДЫЪЧЭЌЯЕЮяЙиЯЕ
ЗжзгзщГЩЯрВювЛИіЉCH2ЉЃЌвђДЫЪЧЭЌЯЕЮяЙиЯЕ
D. ЗжзгЪНЮЊC2H6OЕФКьЭтЙтЦзЭМЩЯЗЂЯжгаCЉHМќКЭCЉOМќЕФеёЖЏЮќЪеЃЌгЩДЫПЩвдГѕВНЭЦВтгаЛњЮяНсЙЙМђЪНЮЊC2H5ЉOH
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЬНОПВнЫсЃЈH2C2O4ЃЉаджЪЃЌНјааШчЯТЪЕбщЁЃЃЈвбжЊЃКЪвЮТЯТЃЌ0.1 molЁЄL1 H2C2O4ЕФpH=1.3ЃЉ
ЪЕбщ | зАжУ | ЪдМСa | ЯжЯѓ |
Ђй |
| Ca(OH)2ШмвКЃЈКЌЗгЬЊЃЉ | ШмвКЭЪЩЋЃЌВњЩњАзЩЋГСЕэ |
Ђк | ЩйСПNaHCO3ШмвК | ВњЩњЦјХн | |
Ђл | ЫсадKMnO4ШмвК | зЯЩЋШмвКЭЪЩЋ | |
Ђм | C2H5OHКЭХЈСђЫс | МгШШКѓВњЩњгаЯуЮЖЮяжЪ |
гЩЩЯЪіЪЕбщЫљЕУВнЫсаджЪЫљЖдгІЕФЗНГЬЪНВЛе§ШЗЕФЪЧ
A. H2C2O4гаЫсадЃЌCa(OH)2+ H2C2O4![]() CaC2O4Ё§+2H2O
CaC2O4Ё§+2H2O
B. ЫсадЃКH2C2O4> H2CO3ЃЌNaHCO3+ H2C2O4![]() NaHC2O4+CO2Ёќ+H2O
NaHC2O4+CO2Ёќ+H2O
C. H2C2O4ОпгаЛЙдадЃЌ2![]() +5
+5![]() +16H+
+16H+![]() 2Mn2++10CO2Ёќ+ 8H2O
2Mn2++10CO2Ёќ+ 8H2O
D. H2C2O4ПЩЗЂЩњѕЅЛЏЗДгІЃЌHOOCCOOH+2C2H5OH![]() C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЛЏбЇЗНГЬЪНЃК![]() ЁЃдкИУЗДгІжаЃЌЦЦЛЕ1mol EGжаЕФЛЏбЇМќашЮќЪеФмСПQ1ЃЌЦЦЛЕ1mol JLжаЕФЛЏбЇМќашЮќЪеФмСПQ2ЃЌаЮГЩ1mol ELжаЕФЛЏбЇМќашЗХГіФмСПQ3ЃЌаЮГЩ1mol JGжаЕФЛЏбЇМќашЗХГіФмСПQ4ШєИУЗДгІЗХГіФмСПЃЌдђЯТСаЙиЯЕЪНвЛЖЈе§ШЗЕФЪЧЃЈ ЃЉ
ЁЃдкИУЗДгІжаЃЌЦЦЛЕ1mol EGжаЕФЛЏбЇМќашЮќЪеФмСПQ1ЃЌЦЦЛЕ1mol JLжаЕФЛЏбЇМќашЮќЪеФмСПQ2ЃЌаЮГЩ1mol ELжаЕФЛЏбЇМќашЗХГіФмСПQ3ЃЌаЮГЩ1mol JGжаЕФЛЏбЇМќашЗХГіФмСПQ4ШєИУЗДгІЗХГіФмСПЃЌдђЯТСаЙиЯЕЪНвЛЖЈе§ШЗЕФЪЧЃЈ ЃЉ
A.Q1+ Q2> Q3+ Q4B.Q1< Q3+ Q4C.Q2< Q3D.Q2< Q4
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯђЪЂгаВЛЭЌЪдМСЕФЪдЙмbжаЗжБ№ЕЮМгЪЪСП0.1mol/L FeCl3 ШмвКЃЌЯТСаЖдbжаЯжЯѓМАНтЪЭе§ШЗЕФЪЧ
ЪЕбщ | bжаЮяжЪ | bжаЯжЯѓ | НсТлЛђНтЪЭ | |
| A | Mg(OH)2 аќзЧвК | гаКьзиЩЋНКЬхВњЩњ | ЗЂЩњЗДгІЃК Fe3++3OH-= Fe(OH)3(НКЬх) |
B | CuЗл | ШмвКБфРЖЃЌЪдЙмЕзВПгаЙЬЬх | ШмвКБфРЖЕФдвђЪЧЃК 3Cu+2Fe3+ =2Fe+3Cu2+ | |
C | 5%H2O2ШмвК | гаЦјХнЩњГЩ | ИУЦјЬхЮЊТШЦјЃЌЫЋбѕЫЎгаЧПбѕЛЏадбѕЛЏCl- ВњЩњCl2 | |
D | БЅКЭNaHCO3ШмвК | гаЦјХнЩњГЩЃЌЧвЪдЙмЕзВПгаЙЬЬх | ЗЂЩњЗДгІЃК Fe3++3HCO3-= Fe(OH)3 +3CO2 |
A. A B. B C. C D. D
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУЕчЛЏбЇЗЈжЦБИLiOHЕФЪЕбщзАжУШчЭМЃЌВЩгУЖшадЕчМЋЃЌaПкЕМШыLiClШмвКЃЌbПкЕМШыLiOHШмвКЃЌЯТСаа№Ъіе§ШЗЕФЪЧЃЈ ЃЉ

AЃЎЭЈЕчКѓбєМЋЧјШмвКpHдіДѓ
BЃЎвѕМЋЧјЕФЕчМЋЗДгІЪНЮЊ4OHЃЈC4eЃЃНO2Ёќ+2H2O
CЃЎЕБЕчТЗжаЭЈЙ§1molЕчзгЕФЕчСПЪБЃЌЛсга0.25molЕФCl2ЩњГЩ
DЃЎЭЈЕчКѓLi+ЭЈЙ§НЛЛЛФЄЯђвѕМЋЧјЧЈвЦЃЌLiOHХЈШмвКДгdПкЕМГі
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com