
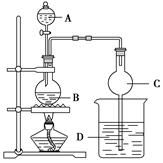
某课外小组设计制备乙酸乙酯的装置如图所示。
查阅资料得到:
Ⅰ.CaCl2可与乙醇生成难溶于水的混合物CaCl2·2C2H5OH;
Ⅱ.数据:
|
物质 |
乙醇 |
乙酸 |
乙酸乙酯 |
浓硫酸(98%) |
|
沸点/℃ |
78.5 |
117.9 |
77.1 |
338.0 |
实验主要步骤如下:
①按图连接好装置(装置气密性良好),A中盛有浓硫酸,B中盛有乙醇和乙酸钠的混合溶液、碎瓷片,D中盛有含酚酞的饱和Na2CO3溶液。
②用小火均匀加热有混合溶液的烧瓶5~10 min。
③待D收集到一定量产物后停止加热,撤出C,将D混合物搅拌,然后静置待分层。
请根据设计要求帮助解决下列问题:
(1)浓硫酸的作用是
________________________________________________________________________。
(2)实验中饱和碳酸钠溶液的作用是(填字母):________。
A.中和乙酸和乙醇
B.中和乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
(3)该小组将教材实验装置图4-2-3(a)进行了改进,一是反应器大试管换成了烧瓶,其优点是________________;二是在导管中添加了球形干燥管,优点是
________________________________________________________________________
________________________________________________________________________。
步骤②中需要小火均匀加热操作,其主要理由是:
________________________________________________________________________
________________________________________________________________________。
(1)做催化剂、吸水剂 (2)BC
(3)受热面积增大,受热均匀 导管插入液面以下,易于乙酸乙酯的冷却,且防止倒吸 减少乙酸和乙醇的挥发,提高其转化率
【解析】
试题分析:该实验同教材实验比较,实验改变(装置、条件、试剂等)处即是其优点:①用圆底烧瓶代换大试管,增大了受热面积,使受热较均匀。②导管末端的球形干燥管插入饱和碳酸钠液面之下易于乙酸乙酯的冷却,也防止了倒吸;饱和碳酸钠溶液的作用简称为“溶解(乙醇)、反应(乙酸)、降低(酯的溶解度)”。若要提高该反应的产率,实验关键是减少副反应的发生,控制好反应的温度,因为乙醇在140 ℃时会生成乙醚,高于这个温度又会产生乙烯或炭化。
考点:考查乙酸乙酯制备、基本实验操作以及实验评价的有关判断
点评:该题是高考中的常见考点和题型,属于中等难度试题的考查,试题基础性强,在注重对学生基础知识巩固和训练的同时,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和规范严谨的实验设计能力。该题的关键是明确乙酸乙酯的制备原理,然后结合题意灵活运用即可。


科目:高中化学 来源: 题型:阅读理解
| ||
| ||


| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 某课外小组在实验室制备氨气,并进行有关氨气的性质探究.
某课外小组在实验室制备氨气,并进行有关氨气的性质探究.查看答案和解析>>
科目:高中化学 来源:黄冈中学2010届高三6月适应性考试理综能力测试化学A卷 题型:实验题
某课外小组在实验室制备氨气,并进行有关氨气的用途及性质的探究。
(1)写出实验室制取氨气的化学方程式: 。
(2)合成氨对化学和国防工业具有重要意义。写出氨的两种重要用途:
① ② 。
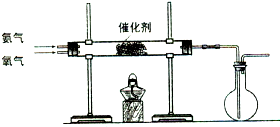
(3)该小组同学设计下图所示装置探究氨气的还原性。

①氨催化氧化的化学方程式为 。
②若实验时通入氨气的速率过快,在烧瓶中会出现白烟,该物质的化学式为 。
(4)该小组同学欲以氨气和二氧化碳为原料制备少量较纯净的碳酸铵溶液设计如下甲 乙两方案。
①甲方案:先将二氧化碳通入水中,充分溶解后,再通入氨气;
乙方案:先将氨气通入水中,充分溶解后,再通入二氧化碳。
合理的方案是: ,理由是 。
②检验产物中有NH4+的方法为 。
③用氢键表示式写出氨水中存在的所有氢键 。
查看答案和解析>>
科目:高中化学 来源:2010年北京市海淀区高三第二次模拟考试(理综)化学部分 题型:实验题
(16分)某课外小组在实验室制备氨气,并进行有关氨气的性质探究。
(1)该小组同学加热生石灰与氯化铵的混合物制取干燥的氨气。

①应该选用的仪器及装置有(填字母) 。
②生石灰与氯化铵反应生成氨气的化学方程式为 。
(2)该小组同学设计如图16所示装置探究氨气的还原性。

①氨催化氧化的化学方程式为 。
②若实验时通入氨气的速率过快,在烧瓶中会出现白烟,该物质的化学式为 。
(3)该小组同学以氨气和二氧化碳为原料制备碳酸氢铵。
①甲同学先将二氧化碳通入水中,充分溶解后,再通入氨气;乙同学先将氨气通入水中,充分溶解后,再通入二氧化碳。再选择合适的方案并说明原因。
②检验产物中有NH4+的方法为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com