

���� �ٸ�����������״���ṹ�жϣ�
�ڷ���е㲻ͬ��Һ̬�����������ķ�����
���÷�Һ©�����з�Һʱ��Ҫ�ȴ��Ͽڲ��������ٴ�������������Һ��˳�����£�
������ƿֻ����������һ��Ũ�ȵ���Һ����ֻ���ڳ�����ʹ�ã�ʹ�ù�����Ҫ��ֹ©ˮ��
��� �⣺������������״��֪BΪԲ����ƿ��EΪ�����ܣ��ʴ�Ϊ��Բ����ƿ�������ܣ�
�ڷ���е㲻ͬ��Һ̬�����������ķ��������õ�������ƿ�������ܣ��ʴ�Ϊ��E��F��
�۷ų�Һ��ʱ��Ӧ���Ͽڲ������������ϵİ��۶�©�����ϵ�С��ʹ��Һ©�����������ͨ�����ֺ�ѹ���÷�Һ©����Һ��˳��������
�ʴ�Ϊ�����ֺ�ѹ���÷�Һ©����Һ��˳��������
������ƿֻ����������һ��Ũ�ȵ���Һ����ֻ���ڳ�����ʹ�ã�ʹ�ù�����Ҫ��ֹ©ˮ��ֻ��CD����Ҫ�ʴ�Ϊ��C��D��
���� ���⿼����������ᴿ��Ϊ��Ƶ���㣬������ѧ���Ļ���ʵ�������Ŀ��飬ע����ճ���������ʹ�÷�����ע�������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
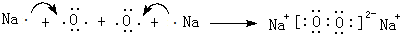 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
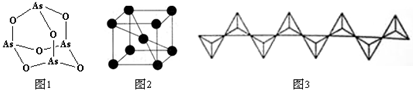
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ױ��������飨���Ը��������Һ�� | B�� | �Ҵ�����ȩ�����ᣨ����Cu��OH��2 | ||
| C�� | �����Ҵ������Ȼ�̼��ˮ�� | D�� | �������顢������Һ��Ũ��ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �۵㣺Li��Na��K | B�� | ��ԭ�ԣ�HCl��H2S��PH3 | ||
| C�� | ����ǿ����H2SiO3��H2CO3��H2SO4 | D�� | ԭ�Ӱ뾶��Na��Mg��Al |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
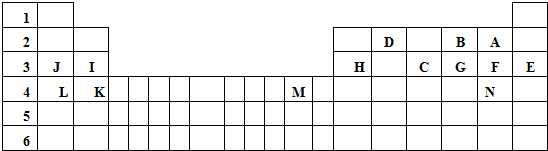
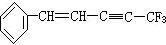 �����У�λ��ͬһƽ���ϵ�ԭ�����������ǣ�������
�����У�λ��ͬһƽ���ϵ�ԭ�����������ǣ�������| A�� | 17 �� | B�� | 18 �� | C�� | 19 �� | D�� | 20 �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 25��ʱ��pH=13�� Ba��OH��2��Һ�к��е�OH-��ĿΪ0.2 NA | |
| B�� | 2.24LCO��CO2�Ļ��������������̼ԭ����һ����NA | |
| C�� | 78g������C=C˫������ĿΪ3NA | |
| D�� | 5.6 g����6.4 gͭ�ֱ���0.1 mol������ȫ��Ӧ��ת�Ƶĵ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
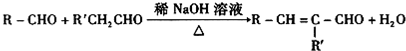
 ��R��R��ɱ�ʾ��������ԭ�ӣ�
��R��R��ɱ�ʾ��������ԭ�ӣ�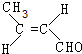 ���÷����������9��ԭ�ӹ�ƽ�森
���÷����������9��ԭ�ӹ�ƽ�森 $��_{��}^{NaOH}$
$��_{��}^{NaOH}$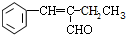 +H2O��
+H2O��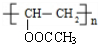 ��
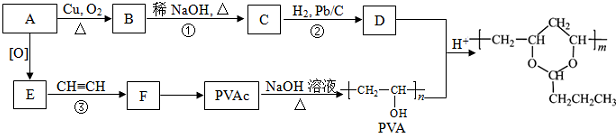
��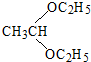 ���ϳ�·������ͼʾ�����£�
���ϳ�·������ͼʾ�����£�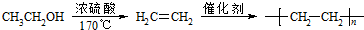
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com