
| A�� | ��Һ1�е������ӿ���NH4+��HCO3-��I-��SO42-��ͬһ��Һ�д������� | |
| B�� | ����Һ2�м���3-5��K3[Fe��CN��6]�����軯�أ���Һ���ɹ۲쵽����ɫ�������� | |
| C�� | �����2�м�������NaOH��Һ��������Ӧ�����ӷ���ʽ��Al��OH��3+OH-=AlO2-+2H2O | |
| D�� | ����Һ2�õ�FeSO4•7H2O��Ʒ�Ĺ����У������������ֹ�������ͷֽ� |
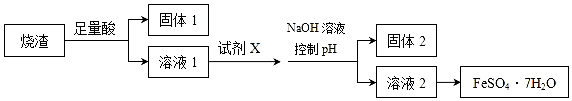
���� ��������ȡ������������Ҫ�ɷ�ΪFe2O3��SiO2��Al2O3���������������ʣ���������м����������ᣬFe2O3��Al2O3���ᷴӦ���ɵ������������������������費��Ӧ�����ˣ�����1Ϊ�������裻����Һ�м������۽������ӻ�ԭΪ�������ӣ�����pHֵʹ��������ȫ���������������������ˣ�����2Ϊ������������Һ2Ϊ��������������Ũ������ȴ�ᾧ�����ˣ��õ������������壬�Դ˽����⣮
��� �⣺A����Һ1�е�������Ϊ�����ӡ������ӣ�����HCO3-��������ˮ�ⷴӦ�����ܴ������棬��������������ӷ���������ԭ��Ӧ����A����
B����Һ2Ϊ�����������������ӿ������軯�ط�����Ӧ������ɫ��������B��ȷ��
C������2Ϊ����������Ϊ�������������NaOH��Һ��Ӧ�����ӷ���ʽΪAl��OH��3+OH-=AlO2-+2H2O����C��ȷ��
D�����������ױ������е���������������������ʧȥ�ᾧˮ�����Դ���Һ2�õ�FeSO4•7H2O��Ʒ�Ĺ����У������������ֹ�������ͷֽ⣬��D��ȷ��
��ѡA��
���� ���⿼���Ʊ�ʵ�鷽������Ϸ����ᴿ��Ϊ�߿��������ͣ����������еķ�Ӧ�����뷽��Ϊ���Ĺؼ�������ѧ�����������ʹ���������������ע����ճ������ʵķ��뷽������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| Ԫ�ش��� | L | M | Q | R | T |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| ��Ҫ���ϼ� | +2 | +3 | +2 | +6��-2 | -2 |
| A�� | �⻯����ȶ���ΪH2T��H2R | |
| B�� | M��T�γɵĻ����������ǿ�ᷴӦ������ǿ�Ӧ | |
| C�� | L2+��R2-����������� | |
| D�� | ���ʷֱ���Ũ����ȵ�ϡ���ᷴӦ������ΪQ��L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 55% | B�� | 60% | C�� | 65% | D�� | 70% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HF���ۡ��е�Ȣ�A������Ԫ���⻯��ĸ� | |
| B�� | ˮ���Ӹ�����Ҳ���ȶ� | |
| C�� | �����ܶȱ�Һ̬ˮ���ܶ�С | |
| D�� | NH3��������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
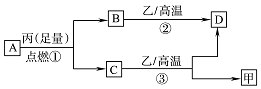 ��֪X��Y��Z������ԭ��������������Ķ�����Ԫ�أ��ס��ҡ����ֱ�������Ԫ���γɵĵ��ʣ�A��B��C��D�ֱ���������Ԫ���е������γɵĻ������A��C�о�����10�����ӣ�����֮��ת����ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
��֪X��Y��Z������ԭ��������������Ķ�����Ԫ�أ��ס��ҡ����ֱ�������Ԫ���γɵĵ��ʣ�A��B��C��D�ֱ���������Ԫ���е������γɵĻ������A��C�о�����10�����ӣ�����֮��ת����ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ԭ�Ӱ뾶��Z��Y��X | B�� | �ȶ��ԣ�A��C | ||
| C�� | ��Ӧ�ں͢۾�Ϊ���ȷ�Ӧ | D�� | X��Y��Z�����γ����ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶�/�� | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
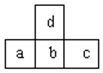
| A�� | d���⻯���b���⻯���ȶ� | |
| B�� | d��c�����γɻ����� | |
| C�� | a��b��c������������Ӧˮ���������ǿ���Ĺ�ϵ��c��b��a | |
| D�� | ԭ�Ӱ뾶�Ĵ�С˳����a��b��c��d |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 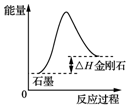 ��ͼ��֪���������Ƕȿ��ǣ����ʯ��ʯī�ȶ� | |
| B�� | 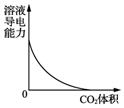 ͼ��ʾCO2ͨ�뱥��Na2CO3��Һ�У���Һ���������ı仯 | |
| C�� | 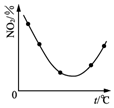 ͼ��ʾ����NO2���ݻ���ͬ�ĺ����ܱ������У���ͬ�¶��·ֱ�����Ӧ��2NO2��g��?N2O4��g������ͬʱ�����NO2���������ߣ���÷�Ӧ�ġ�H��0 | |
| D�� | 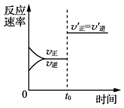 ͼ��ʾij���淴Ӧ�ķ�Ӧ������ʱ��ı仯��t0ʱ�̸ı������һ����ʹ���˴��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
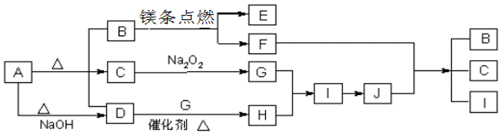
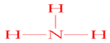 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com