
 ŌŚŗ¬ÓŠČõµē½āÖŹµÄČÜŅŗÖŠ£¬ĶłĶłÓŠ¶ąøö»ÆŃ§Ę½ŗā¹²“ę£®
ŌŚŗ¬ÓŠČõµē½āÖŹµÄČÜŅŗÖŠ£¬ĶłĶłÓŠ¶ąøö»ÆŃ§Ę½ŗā¹²“ę£®·ÖĪö £Ø1£©ČēHAŹĒHCN£¬·“Ó¦ŗóĪŖµČÅØ¶ČµÄHCN”¢NaCNµÄ»ģŗĻČÜŅŗ£¬øł¾ŻČÜŅŗ³ŹµēÖŠŠŌµÄ½Ē¶Č±Č½ĻĄė×ÓÅØ¶Č“óŠ”£»
ČēHAŹĒCH3COOH£¬·“Ó¦ŗóĪŖµČÅØ¶ČµÄCH3COOH”¢CH3COONaµÄ»ģŗĻČÜŅŗ£¬øĆ»ģŗĻČÜŅŗ³ŹĖįŠŌ£¬ĖµĆ÷“×ĖįµÄµēĄė³Ģ¶Č“óÓŚ“×ĖįøłµÄĖ®½ā³Ģ¶Č£»
£Ø2£©ĒāĄė×ÓŅÖÖĘļ§øłĄė×ÓĖ®½ā”¢“×ĖįøłĄė×Ó“Ł½ųļ§øłĄė×ÓĖ®½ā£¬Ņ»Ė®ŗĻ°±ŹĒČõµē½āÖŹ£¬ĻąĶ¬ÅØ¶ČµÄČÜŅŗÖŠŅ»Ė®ŗĻ°±ÖŠļ§øłĄė×ÓÅضČ×īŠ”£»
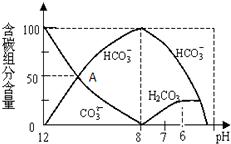
£Ø3£©¢Łøł¾ŻĶ¼ÅŠ¶ĻCŌŖĖŲ“ęŌŚŠĪŹ½£»
¢ŚĖįŠŌĢõ¼žĻĀ£¬ÄÜ“ęŌŚ“óĮæĢ¼Ėį£¬¼īŠŌĢõ¼žĻĀ£¬ÄÜ“ęŌŚ“óĮæĢ¼ĖįøłĄė×Ó£»
¢Ū³£ĪĀĻĀŌŚ20mL0.1mol/L Na2CO3ČÜŅŗÖŠÖšµĪ¼ÓČė0.1mol/L HClČÜŅŗ40mL£¬ĻČ·“Ӧɜ³ÉĢ¼ĖįĒāÄĘ£¬ŌŁÓėŃĪĖį·“Ӧɜ³É¶žŃõ»ÆĢ¼”¢Ė®£¬ŅŌ“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗ£Ø1£©ČēHAŹĒHCN£¬·“Ó¦ŗóĪŖµČÅØ¶ČµÄHCN”¢NaCNµÄ»ģŗĻČÜŅŗ£¬øł¾ŻČÜŅŗµēÖŠŠŌŌŌņæÉÖŖc£ØNa+£©+c£ØH+£©=c£ØCN-£©+c£ØOH-£©£¬ÓÉÓŚc£ØNa+£©£¾c£ØCN-£©£¬Ōņc£ØH+£©£¼c£ØOH-£©£»ČēHAŹĒCH3COOH£¬·“Ó¦ŗóĪŖµČÅØ¶ČµÄCH3COOH”¢CH3COONaµÄ»ģŗĻČÜŅŗ£¬øĆ»ģŗĻČÜŅŗ³ŹĖįŠŌ£¬ĖµĆ÷“×ĖįµÄµēĄė³Ģ¶Č“óÓŚ“×ĖįøłµÄĖ®½ā³Ģ¶Č£¬Ōņc£ØCH3COOH£©£¼c£ØCH3COO-£©£¬
¹Ź“š°øĪŖ£ŗ£¼£»£¼£»
£Ø2£©ĒāĄė×ÓŅÖÖĘļ§øłĄė×ÓĖ®½ā”¢“×ĖįøłĄė×Ó“Ł½ųļ§øłĄė×ÓĖ®½ā£¬Ņ»Ė®ŗĻ°±ŹĒČõµē½āÖŹ£¬ĻąĶ¬ÅØ¶ČµÄČÜŅŗÖŠŅ»Ė®ŗĻ°±ÖŠļ§øłĄė×ÓÅضČ×īŠ”£¬ÅضČĻąµČµÄÕā¼øÖÖČÜŅŗÖŠļ§øłĄė×ÓÅØ¶Č“óŠ”Ė³ŠņŹĒ¢Ś£¾¢Ł£¾¢Ü£¾¢Ū£¬¹Ź“š°øĪŖ£ŗ¢Ś£¾¢Ł£¾¢Ü£¾¢Ū£»
£Ø3£©¢Łøł¾ŻĶ¼ÖŖ£¬ČĖĢåŃŖŅŗµÄpHŌ¼ĪŖ7.4£¬ŌņCO2ŌŚŃŖŅŗÖŠ¶ąŅŌHCO3-µÄŠĪŹ½“ęŌŚ£¬¹Ź“š°øĪŖ£ŗHCO3-£®
¢ŚH2CO3ŹĒ¶žŌŖČõĖį£¬·Ö²½µēĄė£¬µēĄė·½³ĢŹ½ĪŖ£ŗH2CO3?H++HCO3-£¬HCO3-?H++CO32-£¬HCO3-·Ö±šÓėH2CO3”¢CO32-¶¼Äܹ²“ę£¬ĖįŠŌĢõ¼žĻĀ£¬ÄÜ“ęŌŚ“óĮæĢ¼Ėį£¬¼īŠŌĢõ¼žĻĀ£¬“ęŌŚ“óĮæĢ¼ĖįøłĄė×Ó£¬ŅņĪŖ¶žÕß“ęŌŚ»·¾³²»Ķ¬£¬ĖłŅŌH2CO3ŗĶCO32-ŌŚČÜŅŗÖŠ²»ÄÜ“óĮæ¹²“ę£¬
¹Ź“š°øĪŖ£ŗ²»ÄÜ£»
¢ŪĖ®½ā³£ŹżKh=2”Į10-4£¬µ±ČÜŅŗÖŠc£ØHCO3-£©£ŗc£ØCO32-£©=20£ŗ1Ź±£¬c£ØOH-£©=10-3mol/L£¬ÓÉKwæÉÖŖ£¬c£ØH+£©=10-9mol/L£¬ĖłŅŌpH=9£¬¹Ź“š°øĪŖ£ŗ9£®
µćĘĄ ±¾Ģāæ¼²éČõµē½āÖŹµÄµēĄėŗĶŃĪĄąĖ®½ā£¬²ąÖŲæ¼²éѧɜ·ÖĪöÅŠ¶Ļ¼°Ź¶Ķ¼ÄÜĮ¦£¬Ć÷Č·Čõµē½āÖŹµēĄė¼°ŃĪĄąĖ®½āŌĄķŹĒ½ā±¾Ģā¹Ų¼ü£¬ÄѵćŹĒ£Ø2£©ĢāĄė×ÓÅØ¶Č“óŠ”±Č½Ļ£¬ĢāÄæÄѶČÖŠµČ£®


 Ö„ĀéæŖ»ØæĪ³ĢŠĀĢåŃéĻµĮŠ“š°ø
Ö„ĀéæŖ»ØæĪ³ĢŠĀĢåŃéĻµĮŠ“š°ø ŌõѳѧŗĆÅ£½ņÓ¢ÓļĻµĮŠ“š°ø
ŌõѳѧŗĆÅ£½ņÓ¢ÓļĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
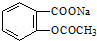 ×Ŗ±äĪŖ
×Ŗ±äĪŖ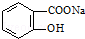 µÄ·½·ØĪŖ£Ø””””£©
µÄ·½·ØĪŖ£Ø””””£©| A£® | ČÜŅŗ¼ÓČČ£¬ĶØČė×ćĮæµÄHCl | |
| B£® | Óė×ćĮæµÄNaOHČÜŅŗ¹²ČČŗó£¬ŌŁĶØČėCO2 | |
| C£® | ÓėĻ”H2SO4¹²ČČŗ󣬼ÓČė×ćĮæµÄNa2CO3 | |
| D£® | ÓėĻ”H2SO4¹²ČČŗ󣬼ÓČė×ćĮæµÄNaOH |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ōö“óŃĪĖįµÄÅØ¶Č | B£® | Ōö“óŃ¹Ēæ | C£® | Ģįøß·“Ó¦µÄĪĀ¶Č | D£® | ÓĆĢś·Ū“śĢęĢśĘ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | c£ØH+£©=10-6 mol•L-1µÄČÜŅŗŅ»¶Ø³ŹĖįŠŌ | |
| B£® | PH=7µÄČÜŅŗŅ»¶Ø³ŹÖŠŠŌ | |
| C£® | c£ØOH-£©=c£ØH+£©µÄČÜŅŗŅ»¶Ø³ŹÖŠŠŌ | |
| D£® | ²»ÄÜŹ¹·ÓĢŖŹŌŅŗ±äŗģµÄČÜŅŗŅ»¶Ø³ŹĖįŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | °±Ė®Ļ”ŹĶŗó£¬ČÜŅŗÖŠ$\frac{c£ØN{{H}_{4}}^{+}£©}{c£ØN{H}_{3}•{H}_{2}O£©}$µÄÖµ¼õŠ” | |
| B£® | 0.1 mol•L-1Na2CO3ČÜŅŗ¼ÓÕōĮóĖ®Ļ”ŹĶ£¬CO32-µÄĖ®½ā³Ģ¶ČŌö“ó£¬ČÜŅŗµÄpH¼õŠ” | |
| C£® | 298 KŹ±£¬2H2S£Øg£©+SO2£Øg£©ØT3S£Øs£©+2H2O£Øl£©ÄÜ×Ō·¢½ųŠŠ£¬ŌņĘä”÷H£¼0 | |
| D£® | ¶ŌN2£Øg£©+3H2£Øg£©ØT2NH3£Øg£©£¬ĘäĖūĢõ¼ž²»±äŹ±³äČėN2£¬Õż·“Ó¦ĖŁĀŹŌö“ó£¬Äę·“Ó¦ĖŁĀŹ¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĶøĆ÷µÄČÜŅŗÖŠ£ŗNa+”¢Cu2+”¢SO42-”¢Cl- | |
| B£® | pH=1µÄČÜŅŗÖŠ£ŗAl3+”¢Mg2+”¢S2O32-”¢AlO2- | |
| C£® | ÄÜŹ¹·ÓĢŖ±äŗģÉ«µÄČÜŅŗÖŠ£ŗFe3+”¢Ba2+”¢HC2O4-”¢Cl- | |
| D£® | ³£ĪĀĻĀ£¬Ė®µēĄėµÄc£ØOH-£©=1”Į10-12mol•L-1ČÜŅŗÖŠ£ŗNH4+”¢Fe2+”¢SO42-”¢NO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ćū³Ę | ŠŌד | ČŪµć£Ø”ę£© | ·Šµć£Ø”ę£© | ĆÜ¶Č£Øg/mL£© | ČܽāŠŌ | |
| Ė® | ŅŅ“¼ | |||||
| ¼×±½ | ĪŽÉ«ŅŗĢåŅ×Č¼Ņ×»Ó·¢ | -95 | 110.6 | 0.8669 | ²»ČÜ | »„ČÜ |
| ±½¼×Ėį | °×ɫʬד»ņÕėד¾§Ģå | 112.4 £Ø100”ę×óÓŅÉż»Ŗ£© | 248 | 1.2659 | Ī¢ČÜ | Ņ×ČÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
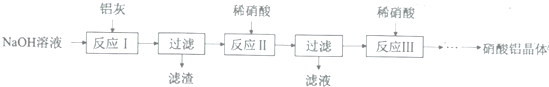
| ĒāŃõ»ÆĪļ | Fe£ØOH£©3 | Al£ØOH£©3 |
| æŖŹ¼³ĮµķpH | 1.9 | 4.2 |
| ³ĮµķĶźČ«pH | 3.2 | 5.4 |
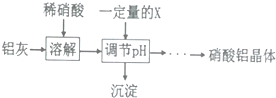
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com