
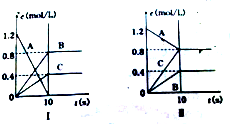
分析 (1)图象分析可知随时间变化,Ⅰ中B、C从0变化为0.4mol/L,0.8mol/L为生成物,A变化为1.2mol/L,Ⅱ中BC增大为生成物,A减小为反应物;
(2)依据图象计算得到ABC变化的浓度,变化量等于化学方程式计量数之比,据此书写化学方程式;
(3)图象分析可知反应的速率匀速进行,计算10s时A的反应速率V(A),6s时变化的A的浓度c(A)=6s×V(A),最后得到A的浓度=1.2mol/L-变化的A的浓度c(A);
解答 解:(1)图Ⅰ、Ⅱ分析图象变化可知,都是A的浓度随反应进行不断减小至不变,BC浓度随反应进行二不断增加至不变化,所以A为反应物,BC为生成物;
故答案为:A,A;
(2)上述分析和图象变化可知,Ⅰ反应中,10s末,A浓度变化为1.2mol/L,B、C的浓度从0变化为0.4mol/L,0.8mol/L,说明该反应不是可逆反应,c(A):c(B):c(C)=1.2:0.4:0.8=3:1:2,反应的化学方程式为:3A=B+2C;Ⅱ反应中,10s末,A浓度变化为1.2mol/L-0.8mol/L=0.4mol/L,B、C的浓度从0变化为0.4mol/L,0.8mol/L,说明该反应不是可逆反应,c(A):c(B):c(C)=0.4:0.4:0.8=1:1:2,反应的化学方程式为:A=B+2C;
故答案为:3A=B+2C,A=B+2C;
(3)在Ⅱ图中图象分析可知反应的速率匀速进行,计算10s时A的反应速率V(A)=$\frac{0.4mol/L}{10s}$=0.04mol/L•s,6s时变化的A的浓度c(A)=6s×V(A)=0.04mol/L•s×6s=0.24mol/L,最后得到A的浓度=1.2mol/L-变化的A的浓度c(A)=1.2mol/L-0.24mol/L=0.96mol/L;
故答案为:0.96mol/L;
点评 本题考查了化学图象分析判断,物质浓度变化和化学方程式书写,注意图象分析和反应速率的理解应用,掌握基础是关键,题目难度中等.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,11.2 L己烷含有分子数为0.5NA | |
| B. | 4.2 g乙烯和环丙烷的混合气体含有H原子数为0.6NA | |
| C. | 甲基(-CH3)的电子总数为10NA | |
| D. | 在常温常压下,2.24 L丁烷和2-甲基丙烷的混合气体所含分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省哈尔滨市高三上学期期中考试化学试卷(解析版) 题型:选择题
一定条件下,在体积为10L的密闭容器中,1molX和1molY进行反应:2X(g)+Y(g) Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是
Z(g),经60s达到平衡,生成0.3molZ。下列说法正确的是
A.0~60s,以X的浓度变化表示的反应速率为0.001mol·L-1·s-1
B.将容器体积变为20L,Z的平衡浓度变为原来的
C.若增大压强,则物质Y的转化率减小
D.若升高温度,X的体积分数增大,则该反应的ΔH>0
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省哈尔滨市高三上学期期中考试化学试卷(解析版) 题型:选择题
水溶液中能大量共存的一组离子是
A.Na+、Al3+、Cl-、CO32-
B.H+、Na+、Fe2+、MnO4-
C.K+、Ca2+、Cl-、NO3-
D.K+、NH4+、OH-、SO42-
查看答案和解析>>
科目:高中化学 来源:2017届河南省南阳市高三上学期第三次月考化学试卷(解析版) 题型:选择题
从某些反应看,NH3和H2O、NH4+和H3O+、NH2—和OH-、N3-和O2-两两类似。据此判断下列反应正确的是
①CaO+2NH4Cl===CaCl2+2NH3↑+H2O②2Na+2NH3===2NaNH2+H2↑
③3Mg(NH2)2===Mg3N2+4NH3↑④NH4Cl+NaNH2===NaCl+2NH3↑
A.只有③
B.只有①
C.①和②
D.都正确
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省长春市高二上学期期初考试化学试卷 题型:选择题
某溶液中存在的离子有Na+、H+、S2-、HS-、OH-,则下列有关该溶液的叙述错误
A.离子浓度可能是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)
B.组成该溶液的溶质只能是Na2S或NaHS或二者的混合物
C.离子物质的量的关系是2n(S2-)+n(HS-)+n(OH-)=n(Na+)+n(H+)
D.该溶液可能呈中性、碱性或酸性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com