
����Ŀ���Խ�����Ʒ���п���ʴ���������ӳ���ʹ������������Ϊ���ı��洦����һ�ַ�����
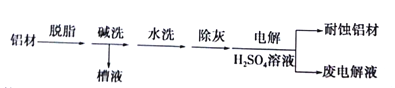
��1����ϴ��Ŀ���dz�ȥ���ı������Ȼ����Ĥ����ϴʱ��������ð����ԭ����______�������ӷ���ʽ��ʾ����Ϊ����ϴ��Һ�е����Գ�����ʽ���գ�������Һ�м��������е�______��
a.![]() b.
b.![]() c.
c.![]() d.
d.![]()
��2��������Ϊ��������![]() ��Һ�е�⣬���ı����γ�����Ĥ�������缫��ӦʽΪ______
��Һ�е�⣬���ı����γ�����Ĥ�������缫��ӦʽΪ______
ȡ�����ϵ��Һ������![]() ��Һ��������ݺͰ�ɫ����������������ԭ����______���û�ѧ����ش�
��Һ��������ݺͰ�ɫ����������������ԭ����______���û�ѧ����ش�
���𰸡�2Al+2OH-+2H2O��2AlO2-+3H2�� a 2Al+3H2O-6e-=Al2O3+6H+ Al3++3HCO3-=Al(OH)3��+3CO2��
��������
��1���ü��ȥ���ĵ�����Ĥʱ��������Ĥ��ȫ�ܽ��¶�������ɼ�����Ӧ���ų�������2Al+2OH-+2H2O��2AlO2-+3H2������ϴ��Һ�к���AlO2-���ɼ�����������ʹ��ת��ΪAl(OH)3������Al(OH)3������ǿ�ᣬ�ʲ���ѡ��HNO3���ʴ���������Ӧ��CO2��
�����������������2Al+2OH-+2H2O��2AlO2-+3H2����a��
��2����������Ϣ��֪����Ϊ������Ҫ���������������ﱣ��Ĥ����������������������Ӧ��Ҫ��������Ĥ��������ˮ�μӣ��ʵ缫��ӦʽΪ��2Al+3H2O-6e-=Al2O3+6H+�����ڵ��Һ�����ᣬ��˵��ʱ���ڵ��Һ�п�������һ��������������������ˮ�������ԣ�̼���������ˮ���Լ��ԣ�������ٽ�������������̼���������������������Ӧ�����ӷ���ʽ��Al3++3HCO3-=Al(OH)3��+3CO2����
����������������ǣ�2Al+3H2O-6e-=Al2O3+6H+��Al3++3HCO3-=Al(OH)3��+3CO2����


 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������100 mL0.020mol/L KMnO4��Һ�Ĺ�������ͼ��ʾ��
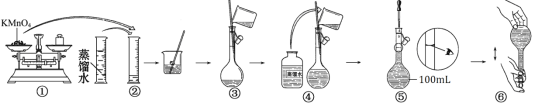
�ش��������⣺
��1��ͼʾ����������������ȷ��������_____��_____ ������ţ���
��2��������ͼʾ�е����������ֱ���________�� __________�������ƣ���
��3�������ͼʾ�IJ���������Һ�������Ƶ���ҺŨ�Ƚ�_______������ƫ��������ƫС������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Fe(OH)3�㷺Ӧ����ҽҩ�Ƽ�������������������Ʊ����輰װ�����£���������ƿ�м���16.7gFeSO4��7H2O��40.0ml����ˮ���߽����������3.0mLŨH2SO4���ټ���2.0gNaClO3���塣ˮԡ������80�棬����һ��ʱ�����NaOH��Һ����ַ�Ӧ�������ˡ�ϴ�ӡ�����ò�Ʒ��
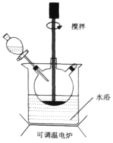
(1)NaClO3����FeSO4��7H2O�����ӷ���ʽΪ_____________��
(2)����Ũ���������Ϊ_________(����)��
a.�ṩ���Ի�������ǿNaClO3������ b.��ȥFeSO4��7H2O�Ľᾧˮ
c.����Fe3+ˮ�� d.��Ϊ������
(3)����Fe2+�Ѿ���ȫ��������ʹ�õ��Լ���_________��
(4)�о���ͬʱ�����¶���NaClO3������Fe2+����Ч����Ӱ�죬��ƶԱ�ʵ�����±�
��� | T/�� | FeSO4��7H2O/g | NaClO3/g | ������/% |
i | 70 | 25 | 1.6 | a |
ii | 70 | 25 | m | b |
iii | 80 | n | 2.0 | c |
iv | 80 | 25 | 1.6 | 87.8 |
��m=______��n=______��
����c>87.8>a����a��b��c�Ĵ�С��ϵΪ___________��
(5)����NaOH��Һ�Ʊ�Fe(OH)3�Ĺ����У�������ˮԡ�¶ȣ�Fe(OH)3�IJ����½�����ԭ����___
(6)�ж�Fe(OH)3����ϴ�Ӹɾ���ʵ�����Ϊ_________________��
(7)���ʵ��֤���ƵõIJ�Ʒ��FeOOH(���費����������)��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������100mL 2mol/L��NaCl��Һ����ش�
��1������ʱ�������NaCl���ʵ���Ϊ____________mol��NaCl���ʵ�����Ϊ____________g��
��2�����ƹ�������Ҫ�õ��������У�ҩ�ס�������ƽ�����롢�ձ�����������____________����ͷ�ιܡ�
��3�����ݵ���ȷ�����ǣ�����������ƿע������ˮ����̶���1-2cm�������ý�ͷ�ι�������ƿ�μ�����ˮ��____________Ϊֹ��
��4������ƿ�ϱ����¶ȡ��̶��ߡ�____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩ��һ����Ҫ�Ļ���ԭ�ϣ���ͨ����ϩ���ѽ��ϩ��״�����Ʊ���
��ϩ���ѽ�������ϩ�ķ�Ӧ����ʽ��2C4H8(g)![]() 2C3H6(g)+ C2H4(g)��
2C3H6(g)+ C2H4(g)��
(1)��֪C4H8��C3H6��C2H4��ȼ���ȷֱ�Ϊ2710.0 kJ![]() mol��1��2050.0 kJ
mol��1��2050.0 kJ![]() mol��1��1410.0 kJ
mol��1��1410.0 kJ![]() mol��1����÷�Ӧ�Ħ�H��_______ kJ
mol��1����÷�Ӧ�Ħ�H��_______ kJ![]() mol��1�����в����������C4H8��ƽ��ת���ʣ����ܼӿ췴Ӧ���ʵ���_________��
mol��1�����в����������C4H8��ƽ��ת���ʣ����ܼӿ췴Ӧ���ʵ���_________��
A�������¶� B������ѹǿ
C������C4H8��Ũ�� D��ʹ�ø���Ч�Ĵ���
(2)ij�¶��£������Ϊ2 L�ĸ����ܱ������г���2.00 mol C4H8����������Ӧ�������ڵ���ѹǿp��ʱ��t�ı仯���±���ʾ��
��Ӧʱ��t/min | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
��ѹǿp/kPa | 4.00 | 4.51 | 4.80 | 4.91 | 4.96 | 5.00 | 5.00 |
��0~10 min����(C4H8)��_______ mol![]() L��1
L��1![]() min��1�����¶��µ�ƽ�ⳣ��K��_______kPa��������ķ�ѹ��ʾ����
min��1�����¶��µ�ƽ�ⳣ��K��_______kPa��������ķ�ѹ��ʾ����
���״�ת����ϵ���ϩ�ѽ������������ϩ����Ҫ�漰���з�Ӧ��
�� 2C4H8(g)![]() 2C3H6(g)+ 2H4(g) ��H��0
2C3H6(g)+ 2H4(g) ��H��0
�� 2CH3OH(g)![]() C2H4(g) + 2H2O(g) ��H��0
C2H4(g) + 2H2O(g) ��H��0
�� C2H4(g)+ C4H8(g)![]() 2C3H6(g) ��H��0
2C3H6(g) ��H��0
��֪���״������ڴ����ϣ����Ի�������״�Ũ�ȹ���Ҳ�����ƶ�ϩ�ڴ����ϵ�ת����
(3)ͼ1��C3H6��ijЩ������IJ�����n(CH3OH)/n(C4H8)�Ĺ�ϵ���ߡ���ѵ�n(CH3OH)/n(C4H8)ԼΪ_________��

(4)ͼ2��ijѹǿ�£���CH3OH��C4H8��һ�������ʵ���֮��Ͷ�ϣ���Ӧ�ﵽƽ��ʱC3H6������������¶ȵı仯���ߡ���ͼ��֪ƽ��ʱC3H6������������¶ȵ����߳��������ߺͣ���ԭ�������__________________________________________________��

(5)�����йؽ��״�ת����ϵ���ϩ�ѽ������������ϩ��˵����ȷ����________��
A������״���ͨ����һ�����Դٽ���ϩ�ѽ�
B���״�ת�����ɵ�ˮ���Լ��ٴ����ϵĻ�̼���ӳ�����������
C����״��붡ϩ�����ʵ����ı�ֵ������߱�ϩ��ƽ�����
D�����״�ת�����붡ϩ���ѽ��У�����ʵ�ַ�Ӧ��ЧӦƽ�⣬�����ܺ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���ĽṹΪ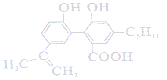 ������˵����ȷ���ǣ� ��
������˵����ȷ���ǣ� ��
A. 1 mol���л�����������7 mol H2�����ӳɷ�Ӧ
B. ���л�����Է���ȡ�����ӳɡ�������ˮ��ȷ�Ӧ
C. 0.1 mol���л��������������Ʒ�Ӧ����������3.36L H2
D. ����л��������ͬ�����ŵ�ͬ���칹�干��8�֣������������칹��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ�ſ��ܷ�����ѧ��Ӧ����Щ���ӱ���Ϊ����ӡ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λͨ����kJmol��1��ʾ��������۲�ͼ1��Ȼ��ش����⡣
��1��ͼ����ʾ��Ӧ��________��������������������������Ӧ��

��2����֪��1mol H��H����1mol I��I��1mol H��I���ֱ���Ҫ���յ�����Ϊ436kJ��151kJ��299kJ������1mol������1mol �ⷴӦ����HI��________�������ų���������������________kJ���������ڻ�ѧ��Ӧ�����У��ǽ�________ת��Ϊ________��
��3��ijʵ��С��ͬѧ������ͼ2��ʵ�飬��̽����ѧ��Ӧ�е������仯��ʵ����������е��¶Ƚ��ͣ��ɴ��ж����������������Ȼ�茶��巴Ӧ��________��������������������������Ӧ��ʵ�����У���С��ͬѧ���ձ��м���5mL 1.0mol/L���ᣬ�ٷ�����ɰֽ��ĥ�����������÷�Ӧ��________��������������������������Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Xֻ������A1����NH4)2SO4 ��MgCl2��FeCl2, AlCl3�е�һ�ֻ�����ɣ�ijͬѧ�Ըù������������ʵ��

�����ж���ȷ����
A.�����һ���Ǵ�����B.����X��һ��������FeCl2
C.��ɫ���������ǻ����D.����X��һ������AlCl3��(NH4)2SO4, MgCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪25��ʱ����������ʵĵ���ƽ�ⳣ�����������ʾ���ش��������⣺
��ѧʽ | CH3COOH | H2CO3 | HClO | |
����ƽ�ⳣ�� | Ka��1.8��10��5 | Kal��4.3��10��7 | Ka2��5.6��10��11 | Ka��3.0��10��8 |
(1) a��CH3COONa b��Na2CO3c��NaClO d��NaHCO3������Һ�����ʵ���Ũ�Ⱦ�Ϊ0.1mol��L��1�ģ�pH��С�������е�˳����_______________(�ñ����д)��
(2)�����£�0.1mol��L��1CH3COOH��Һ��ˮϡ�����У����б���ʽ�����ݱ�������______��
A��c(H��) B��c(H��)/c(CH3COOH) C��c(H��)��c(OH��)
D��c(OH��)/c(H��) E��c(H��)��c(CH3COO��)/c(CH3COOH)
(3)�����Ϊ100mL pH��2��CH3COOH��һԪ��HX����ˮϡ������pH����Һ����Ĺ�ϵ��ͼ��ʾ����HX�ĵ���ƽ�ⳣ��_____(����ڡ�����С�ڡ����ڡ�)CH3COOH�ĵ���ƽ�ⳣ����������_____________________��

(4)25��ʱ��CH3COOH��CH3COONa�Ļ����Һ�������pH��6������Һ��
c(CH3COO��)��c(Na��)��___________________mol��L��1(�ȷֵ)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com