

分析 根据题中各物质转化的关系及条件,A在浓硫酸作用下发生消去反应,应为醇的消去,根据1,3-丁二烯的结构可知,A为HOCH2CH2CH2CH2OH,所反应X应为丁炔二醇与氢气的加成反应,反应的试剂及条件为氢气、催化剂,A生成B为取代反应,B发生消去反应得1,3-丁二烯,可知A与溴化氢取代生成B为BrCH2CH2CH2CH2Br,反应的试剂及条件为,B在氢氧化钠的醇溶液中发生消去反应得1,3-丁二烯,反应的试剂及条件为氢氧化钠醇溶液、加热,据此答题.
解答 解:根据题中各物质转化的关系及条件,A在浓硫酸作用下发生消去反应,应为醇的消去,根据1,3-丁二烯的结构可知,A为HOCH2CH2CH2CH2OH,所反应X应为丁炔二醇与氢气的加成反应,反应的试剂及条件为氢气、催化剂,A生成B为取代反应,B发生消去反应得1,3-丁二烯,可知A与溴化氢取代生成B为BrCH2CH2CH2CH2Br,反应的试剂及条件为溴化氢、加热,B在氢氧化钠的醇溶液中发生消去反应得1,3-丁二烯,反应的试剂及条件为氢氧化钠醇溶液、加热,
(1)根据上面的分析可知,反应X的试剂及条件为氢气、催化剂,反应Y的试剂及条件为溴化氢、加热,反应Z的试剂及条件为氢氧化钠醇溶液、加热,
故答案为:氢气、催化剂;溴化氢、加热;氢氧化钠醇溶液、加热;
(2)根据上面的分析可知,A为HOCH2CH2CH2CH2OH,B为BrCH2CH2CH2CH2Br,
故答案为:HOCH2CH2CH2CH2OH;BrCH2CH2CH2CH2B;
(3)丁炔二醇→A的化学方程式为HOCH2C≡CCH2OH+2H2$\stackrel{催化剂}{→}$HOCH2CH2CH2CH2OH,A→1,3-丁二烯的化学方程式为HOCH2CH2CH2CH2OH$→_{△}^{浓硫酸}$CH2=CHCH=CH2+2H2O,
故答案为:HOCH2C≡CCH2OH+2H2$\stackrel{催化剂}{→}$HOCH2CH2CH2CH2OH;HOCH2CH2CH2CH2OH$→_{△}^{浓硫酸}$CH2=CHCH=CH2+2H2O;
点评 本题考查有机物物的合成与推断,题目难度不大,注意把握有机物官能团的变化以及反应条件,本题可用正推的方法进行推断.


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:解答题
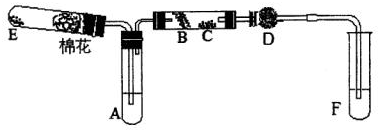
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 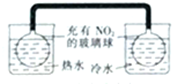 左边玻璃球内气体颜色更浅 | B. | 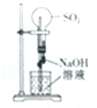 挤压胶头滴管产生喷泉现象 | ||
| C. | 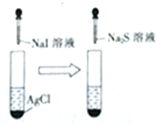 白色沉淀先变黄色再变黑色 | D. | 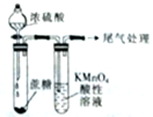 酸性高锰酸钾溶液褪色或变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
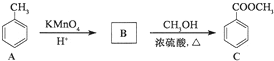
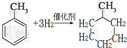 ,反应类型为加成反应.
,反应类型为加成反应.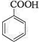 ,所得B的粗产品通常用重结晶的方法提纯.
,所得B的粗产品通常用重结晶的方法提纯.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
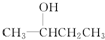 D.
D.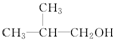 E.
E.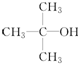
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②⑤ | C. | ②③⑤ | D. | ②③④⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com