
����Ŀ����֪ij���ĺ���������A�ܷ���������ʾ�ı仯������ͬ�����£�A���ܶ���H2��28��������̼����Ԫ�ص���������֮��Ϊ71.4%��C��ʹ������Ȼ�̼��Һ��ɫ��H�Ļ�ѧʽΪC9H12O4 �� 
�Իش��������⣺
��1��A�к��������ŵ�������C�Ľṹ��ʽ ��
��2��D���ܷ����ķ�ӦΪ�����ţ���
��������Ӧ �ڼӳɷ�Ӧ ����ȥ��Ӧ �ܼӾ۷�Ӧ
��3��д�����з�Ӧ�ķ���ʽ��A��������Һ������G��H����
��4��ij�����廯����M����A������ͬ���ͺ���Ŀ�Ĺ����ţ�����Է���������A��76����
��M�Ļ�ѧʽΪ��
����֪M��ͬ���칹��Ϊ�����廯�������FeCl3��Һ������ɫ��Ӧ��������Na��Ӧ���ҹ����Ų�ֱ����������M��ͬ���칹��Ϊ��д1�֣��� ��
���𰸡�
��1��ȩ����CH2=CHCH2OH
��2���٢�
��3��![]() ��
��
��4��C9H8O��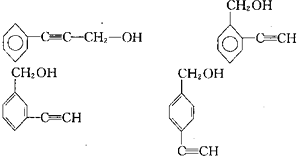
���������⣺���ܶȵĹ�ϵ���Ƴ�A����Է�������Ϊ56����A��B�ķ�Ӧ����֪A�к���ȩ������C��ʹ������Ȼ�̼��Һ��ɫ��B��D�ķ�Ӧ�����Ƴ�A�к���̼̼˫���������á��л������Ƴ�A�Ľṹ��ʽΪCH2=CHCHO��A��ȩ��������Ϊ�Ȼ���ΪB��BΪCH2=CHCOOH��B��HBr�ӳɵõ�D��DΪBrCH2CH2COOH��D��Br����ȡ����Ӧ����E��EΪHOCH2CH2COOH��E�Щ�OH����������Ӧ�õ�F��FΪOHCCH2COOH��ȩ���ٱ�����ΪG��GΪHOOCCH2COOH��A��C��ȩ������ԭ��C�Ľṹ��ʽΪCH2=CHCH2OH��G��C��Ӧ������Ӧ�õ�H��HΪCH2=CHCH2OOCCH2COOCH2CH=CH2 �� ��1��ͨ�����Ϸ���֪��A�Ľṹ��ʽΪ��CH2=CHCHO������A�к�����������ȩ����C�Ľṹ��ʽΪCH2=CHCH2OH�����Դ��ǣ�ȩ����CH2=CHCH2OH����2��DΪBrCH2CH2COOH��������ԭ�Ӻ��Ȼ��������ܷ���������Ӧ����ȥ��Ӧ����ѡ�٢ۣ���3��A��������Һ����������Ӧ����Ӧ����ʽΪ�� ![]() ��������ͱ�ϩ������������Ӧ����Ӧ����ʽΪ��
��������ͱ�ϩ������������Ӧ����Ӧ����ʽΪ��  �����Դ��ǣ�
�����Դ��ǣ� ![]() ��
�� 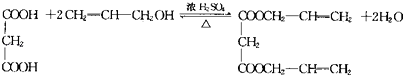 ����4����A�Ľṹ��ʽΪCH2=CHCHO��ij�����廯����M��˵��M�к��б�����һ��������ʽ����77��A��ʽ����55����A������ͬ���ͺ���Ŀ�Ĺ����ţ�˵��A�к���̼̼˫����ȩ��������Է���������A��76������A�ķ���ʽΪC9H8O�����Դ��ǣ�C9H8O��
����4����A�Ľṹ��ʽΪCH2=CHCHO��ij�����廯����M��˵��M�к��б�����һ��������ʽ����77��A��ʽ����55����A������ͬ���ͺ���Ŀ�Ĺ����ţ�˵��A�к���̼̼˫����ȩ��������Է���������A��76������A�ķ���ʽΪC9H8O�����Դ��ǣ�C9H8O��
��M��ͬ���칹��Ϊ�����廯���˵�����б���������FeCl3��Һ������ɫ��Ӧ��˵���������ǻ���������Na��Ӧ��˵�����д��ǻ����ҹ����Ų�ֱ����������ýṹ�к���̼̼������������ṹ��ʽΪ�� 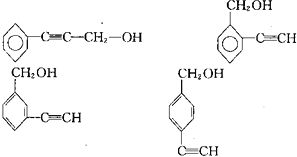 �����Դ��ǣ�
�����Դ��ǣ�  ��
��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ҫ����2mol/L��NaCl��Һ980 ml������ʱӦѡ�õ�����ƿ�Ĺ��ͳ�ȡ��NaCl�������ֱ����� ��
A. 980 mL��114.7g B. 500mL�� 58.5g
C. 1000 mL�� 117 g D. 1000mL��117.0g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�������У���ij��̼ԭ���������ĸ���ͬ��ԭ�ӻ�ԭ���ţ������̼ԭ�ӱ���Ϊ������̼ԭ�ӡ�������������̼ԭ�ӵ�����һ�����й�ѧ���ԣ����л���й�ѧ���ԣ��������з�Ӧ�����ɵ��л������й�ѧ���Ե��ǣ� ��
������ᷢ��������Ӧ
����NaOH��Һ��Ӧ
����������Һ����
���ڴ�����������H2���ã�![]()
A.�ڢ�
B.�٢�
C.�٢�
D.�ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȫ��������ԭ�����һ�����Ϳɳ��أ���ͬ��̬�ĺ���������Ϊ���������Ļ������ʣ��ֱ��ڸ��Ե����Ե��Һ�����С���ṹԭ����ͼ��ʾ���õ�طŵ�ʱ���Ҳ��еĵ缫��ӦΪ��V2+-e-=V3+������˵����ȷ����
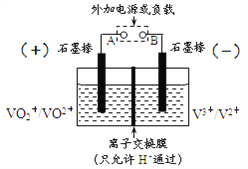
A. �ŵ�ʱ���Ҳ۷�����ԭ��Ӧ
B. �ŵ�ʱ����۵ĵ缫��Ӧʽ��VO2++2H++e-=VO2++H2O
C. ���ʱ��ÿת��1mol���ӣ�n(H+)�ı仯��Ϊ1mol
D. ���ʱ���������ҺpH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��ij��ͬѧ������ʵ��̽��Fe2+��Fe3+�����ʡ��ش��������⣺
��1���ֱ�ȡһ�����Ȼ������Ȼ��������壬�����Ƴ�0.1 mol/L ����Һ����FeCl2��Һ�������������м����Ŀ����__________________________��
��2������ͬѧȡ2mLFeCl2��Һ�����뼸����ˮ���ټ���1��KSCN��Һ����Һ��죬˵��Cl2�ɽ�Fe2+������FeCl2��Һ����ˮ��Ӧ�����ӷ���ʽΪ_______________��
��3������ͬѧ��Ϊ�����ʵ�鲻���Ͻ�������ͬѧ��2mLFeCl2��Һ���ȼ���0��5mLú�ͣ�����Һ�������μ��뼸����ˮ��1��KSCN��Һ����Һ��죬ú�͵�������_____________��
������������(��Ҫ�ɷ�ΪAl2O3��������SiO2��Fe2O3)�ǹ�ҵ���Ʊ�����������Ҫԭ�ϣ���ҵ����ȡ�������Ĺ����������£�

(1)����A�ijɷ��ǣ��ѧʽ��_________��
(2)������м������NaOH��Һ������Ӧ�����ӷ���ʽ������H++OH��=H2O���У�
_____________________________��________________________________��
(3)�������ͨ�����CO2��������ӷ���ʽ��______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£��̶��ݻ����ܱ������У���Ӧ2SO2(g)+O2(g)![]() 2SO3(g)���ﵽ��ѧƽ��״̬�ı�־��
2SO3(g)���ﵽ��ѧƽ��״̬�ı�־��
��n(SO2)��n(O2)��n(SO3) =2��1��2 ��SO2��Ũ�Ȳ��ٷ����仯 �������е�ѹǿ����
�ܵ�λʱ��������nmolSO3��ͬʱ����2nmolO2 �ݻ�������ƽ����Է�����������
A. �٢ܢ� B. �٢ڢ� C. �ڢۢ� D. �٢ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��л����������ɡ����ʵ�˵������ȷ�ģ�������
A.��Ȼ����Һ��ʯ�����ijɷ���ͬ
B.�����ǡ����ۺ�����������һ�������¶��ܷ���ˮ�ⷴӦ
C.���ۡ������ʾ����ڸ߷��ӻ��������֬�����ڸ߷��ӻ�����
D.ʯ�͵��ѽ��ǻ�ѧ�仯����ʯ�͵ķ����ú�ĸ����������仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����³�ѹ����2L�ĺ����ܱ�������Ͷ��2mol A��1mol B���������淴Ӧ 3A��g��+2B��s��2C��g��+D��g����H=��a kJ/mol��5min���ƽ�⣬���������n��C��=0.8mol��������˵����ȷ���ǣ� ��
A.3v��A��=2v��C��=0.16 mol/��Lmin��
B.�ÿ��淴Ӧ��ƽ��ų�0.8a kJ�����ܣ����軯ѧ��ȫת��Ϊ���ܣ�
C.�����¶ȣ���ƽ���������ʼ�С����ƽ�������ƶ�
D.ʹ�ô�������С�����������ƽ��������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͭ��һ����Ũ���ᷴӦ���õ�����ͭ��Һ��NO2��N2O4��NO�Ļ�����壬��Щ������2.24LO2(��״��)��Ϻ�ͨ��ˮ�У�����������ȫ��ˮ�����������ᡣ������������ͭ��Һ�м���2 mol/L NaOH��Һ��Cu2��ǡ����ȫ������������NaOH��Һ�������( )
A. 60 mL B. 50 mL
C. 45 mL D. 15 mL
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com