
【题目】常溫下,浓度均为1.0mol/L的HX溶液、HY溶液、HY和 NaY的混合溶液,分别加水稀释,稀释后溶液的pH随浓度的变化如图所示,下列叙述正确的是( )
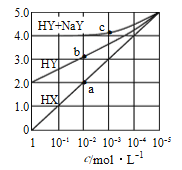
A. HX是强酸,溶液每稀释10倍,pH始终增大1
B. 常温下HY的电离常数为1.0×10-4
C. 溶液中水的电离程度:a点大于b点
D. c 点溶液中:c(Na+)>c(Y-)>c(HY)>c(H+)>c(OH-)
科目:高中化学 来源: 题型:
【题目】下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向FeBr2溶液中通入适量Cl2,溶液由浅绿色变为黄色 | Cl2氧化性强于Br2 |
B | 常温下,等体积pH=3的HA和HB两种酸分别加水稀释,溶液导电能力如图
| HA酸性比HB弱 |
C | 向无水乙醇中加入浓H2SO4,加热,将产生的气体通入酸性KMnO4溶液,紫红色褪去 | 反应产生乙烯 |
D | 取久置的Na2O2粉末,向其中滴加过量的盐酸,产生无色气体 | 气体为氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室制取少量乙酸乙酯的装置图。下列关于该实验的叙述中,不正确的是

A. 试管b中导气管下端管口不能浸入液面的原因是防止实验过程中发生倒吸现象
B. 向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸
C. 实验时加热试管a的目的是及时将乙酸乙酯蒸出并加快反应速率
D. 试管b中Na2CO3的作用是除去随乙酸乙酯蒸出的少量乙酸和乙醇,降低乙酸乙酯在溶液中溶解度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀工业会产生大量的电镀污水,处理某独酸性电镀废液(主要含Cu2+、Fe3 +)以制备氯化亚铜的工艺流程如图所示:

已知:① 氯化亚铜(CuCl)是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化成绿色碱式盐。
② 常温下,
物质 | Fe(OH)3 | Cu(OH)2 |
Kap | 4.0×10-38 | 5.0×10-20 |
请回答下列问题:
(1)加H2SO4的步骤中,下列措施,可提高溶解速率的是_______(填序号)。
a.加热 b.增大压强 c.延长浸出时间 d.适当提高硫酸的浓度
(2)电镀污泥的主要成分是____,产品CuCl晶体要用无水乙醇洗涤、真空干燥、密封包装的目的是______________。
(3)加入H2SO4的目的是_________。
(4)亚硫酸钠、氯化钠、硫酸铜在溶液中反应生成CuCl的离子方程式为__________。
(5)实验探究pH对CuCl产率的影响如图 所示,当pH=2时CuCl 产率最大的原因是_________

(6)以碳棒为电极电解CuCl2溶液也可得到CuCl。写出电解CuCl2溶液阴极的反应方程式:_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)工业上可以采用热还原法制备金属镁(镁沸点为1107℃,熔点是648.8℃)。
(1)将碱式碳酸镁[4MgCO3·Mg(OH)2·5H2O]和焦炭按一定比例混合,放入真空管式炉中先升温至500℃保持一段时间,然后升温至1450℃反应制得镁。
①用碳还原法制备金属镁需要在真空中而不在空气中进行,其原因是 。
②焦炭与碱式碳酸镁的物质的量的比值不同对镁的还原率有较大影响,结果如图。当比值大于15∶1时,还原率下降的原因可能是 。
③碱式碳酸镁分解如图所示,写出在1450℃反应制得镁的化学反应方程式 。


(2)工业上可以采用MgCl2溶液和Na2CO3溶液混合制备碱式碳酸镁,写出反应离子方程式 。
反应采用68℃,温度不宜高于68℃的原因是 。
(3)工业采用电解MgCl2溶液产生Mg(OH)2,如图。然后用Mg(OH)2悬浊液吸收烟气中的二氧化碳,减少二氧化碳的排放同时产生碱式碳酸镁。该电池的阴极电极反应式为 。电解时还得到副产物为 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成气(主要成分为CO、CO2和H2)是重要的化工原料,可利用合成气在催化剂存在下直接制备二甲醚(CH3OCH3)。
己知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.0kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.0kJ·mol-1
CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2=+41.1 kJ·mol-1
CO(g)+H2O(g) △H2=+41.1 kJ·mol-1
2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H3=-24.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H3=-24.5 kJ·mol-1
(1)工业上用CO2和H2在一定条件下反应直接制备二甲醚,主反应为: 2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)
①要使该反应速率和产率都增大,应该采取的措施是__________,减少副反应,大幅度提高二甲醚在产物中所占比率的关键因素是__________。
②一定条件下.上述主反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是__________(单选,填标号)。
a.逆反应速率先增大后减小 b.H2的转化率增大
c.反应物的体积百分含量减小 d.容器中的![]() 变小
变小
③在某压强下,制备二甲醚的反应在不同温度、不冋投料比时CO2的转化率如图(a)所示。T1温度下,将6molCO2和12molH2充入10L的密闭容器中, 5 min后反应达到平衡状态,则05 min内的平均反应速率v(CH3OCH3)=_____________;KA、 KB、 KC三者之间的大小关系为_______________。

(2)在适当条件下由CO和H2直接制备二甲醚,另一产物为水蒸气。
①该反应的热化学方程式是_________________。
②co的转化率、二甲醚的产率与反应温度的关系如图(b)所示,请解释温度低于290℃时, CO转化率较高而CH3OCH3产率较低的原因可能是___________。

(3)用甲醇,二甲醚混合液与CO在催化剂条件下还可合成醋酸。常温下,醋酸的Ka=1.8×10-5,向 0.1 mol/L 醋酸溶液中滴加NaOH溶液至 =
=![]() 时,混合溶液的pH=__________,醋酸钠水解反应的平衡常数值为__________。
时,混合溶液的pH=__________,醋酸钠水解反应的平衡常数值为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油分馏塔装置示意如图。a、b、c分别为石油分馏产品。下列说法正确的是

A. 在a、b、c三种馏分中,a的熔点最高
B. 分馏产品的沸点:a>b>c>柴油>重油
C. 在a、b、c三种馏分中,c的平均相对分子质量最大
D. a、b、c、柴油、重油都是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家研究发现,具有高度对称性的有机分子具有致密性高,稳定性强,张力能大等特点,因此这些分子成为2014年化学界关注的热点,下面是几种常见高度对称烷烃的分子碳架结构,这三种烷烃的二氯取代产物的同分异构体数目分别是(不考虑立体异构)

A. 1种,3种,5种 B. 1种,2种,6种
C. 1种,3种,8种 D. 2种,3种,8种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,用浓度为0.100 0 mol·L-1的氢氧化钠溶液分别滴定20.00 mL浓度均为0.100 0 mol·L-1的二种酸HX、HY(忽略体积变化),实验数据如下表,下列判断不正确的是 ( )
数据编号 | 滴入NaOH(aq) 的体积/mL | 溶液的pH | |
HX | HY | ||
① | 0 | 3 | 1 |
② | a | 7 | x |
③ | 20.00 | >7 | y |
A. 在相同温度下,同浓度的两种酸溶液的导电能力:HX<HY
B. 由表中数据可估算出Ka(HX)≈10-5
C. HY和HX混合,c(H+)=c(X-)+c(Y-)+c(OH-)
D. 上述②反应后的HY溶液中:c(Na+)>c(Y-)>c(OH-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com