
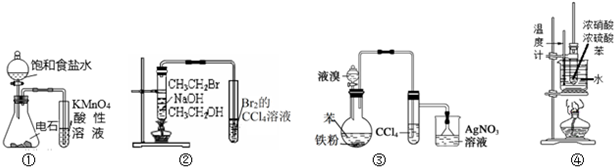
| A. | 装置①可用于检验乙炔的还原性 | |
| B. | 装置②可以证明CH3CH2Br发生消去反应生成了乙烯 | |
| C. | 装置③可以证明苯生成溴苯的反应是取代反应 | |
| D. | 装置④可用于实验室制备硝基苯 |
分析 A.乙炔中含有杂质,发生生成硫化氢;
B.乙烯能与溴单质发生加成;
C.在催化剂的作用下,苯环上的氢原子被溴原子所取代,生成溴苯,同时有溴化氢生成,硝酸银为检验生成的溴化氢,利用溴化氢电离出的溴离子和银离子反应,生成淡黄色不溶于硝酸的沉淀溴化银;
D.制取硝基苯应该用水浴加热.
解答 解:A.乙炔中含有杂质,发生生成硫化氢,硫化氢有还原性,能使酸性高锰酸钾褪色,故A错误;
B.乙烯能与溴单质发生加成,使溴的四氯化碳溶液褪色,故B正确;
C.在催化剂的作用下,苯环上的氢原子被溴原子所取代,生成溴苯,同时有溴化氢生成,硝酸银为检验生成的溴化氢,利用溴化氢电离出的溴离子和银离子反应,生成淡黄色不溶于硝酸的沉淀溴化银,由此来检验溴和苯发生了取代反应,故C正确;
D.制取硝基苯时温度为55~60℃,应该用水浴加热,不能直接加热,故D正确.
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及乙炔的还原性、消去和取代反应、硝基苯的制取等知识点,明确实验原理是解本题关键,能从实验操作规范性、操作评价性分析解答,题目难度不大.


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | 反应在水溶液中进行时,若A为金属,则B一定是金属 | |
| B. | 反应在水溶液中进行时,若A为非金属,则B一定是非金属 | |
| C. | 反应在加热或高温下进行时,若A为金属,则B一定是非金属 | |
| D. | 反应在加热或高温下进行时,若A为非金属,则B一定是金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -2 |
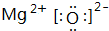 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与冷水反应 | B. | Ba(OH)2•8H2O与NH4Cl的反应 | ||
| C. | 灼热的炭与CO2的反应 | D. | 铝与氧化铁的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2是很好的抑菌剂,红酒中常加人微量的SO2 | |
| B. | 麦片中常加人微量铁粉,可以防止被氧化而变质 | |
| C. | “PM2.5“是指大气中直径≤2.5微米的颗粒物.其悬浮在空气中一定形成气溶胶 | |
| D. | 制饭勺、饭盒、高压锅等的不锈钢是合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一氧化碳极易与血红蛋白结合,所以有毒 | |
| B. | 氧气易溶于水,所以鱼能生存 | |
| C. | 金刚石和石墨都是碳元素组成的单质,所以性质相似 | |
| D. | 溶液由溶质和溶剂组成,所以溶液体积等于溶质体积加溶剂体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
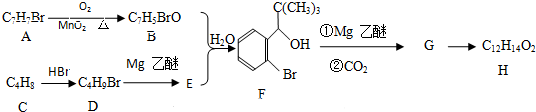
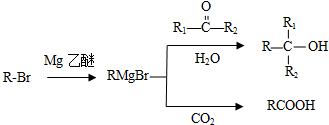
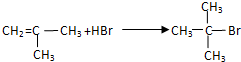 ;G→H
;G→H .
.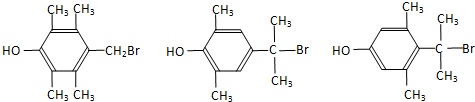 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀释pH=3的醋酸,溶液中所有离子的浓度均降低 | |
| B. | 相同条件下,pH=5的①NH4C1溶液、②CH3C00H溶液、③稀盐酸溶液中由水电离出的c(H+):①>②>③ | |
| C. | 体积相同、浓度均为0.1mol/L的盐酸和醋酸,分别稀释m倍、n倍,溶液的pH都变成5,则m<n | |
| D. | pH=5的硫酸溶液稀释到原来的500倍,稀释后溶液中的c(SO42-)与c(H+)之比约为1:10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com