
| V |
| Vm |
| 1 |
| 2 |
| n |
| V |
| 0.2mol×1 |
| 1 |
| 3.36L |
| 22.4L/mol |
| 1 |
| 2 |
| 1 |
| 2 |
| 0.15mol |
| 0.1L |
| 0.05mol |
| 0.1L |


科目:高中化学 来源: 题型:
| A、在任何物质分子中都含有化学键 |
| B、形成离子键的阴阳离子间只存在静电吸引力 |
| C、D2O分子与H2O分子是所含电子总数不相等的分子 |
| D、CO2、PCl3分子中所有原子都满足最外层8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
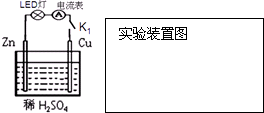 (1)原电池是一种将
(1)原电池是一种将查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.请回答:
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
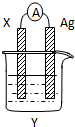 依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com