
| A. | 通过煤的直接或间接液化可以获得各种芳香烃 | |
| B. | 通过石油的催化重整等工艺可获取芳香烃 | |
| C. | 石油的裂化的目的主要是为了提高轻质油的产量 | |
| D. | 石油的裂解的目的主要是为了获取不饱和烯烃 |
分析 A、煤的液化不能获得芳香烃;
B、催化重整是在加热、加压和催化剂存在的条件下,使原油蒸馏所得的轻汽油馏分(或石脑油)转变成富含芳烃的高辛烷值汽油(重整汽油),并副产液化石油气和氢气的过程;
C、石油裂化的目的是为了提高轻质液体燃料的产量,特别是提高汽油的产量;
D、石油裂解的目的是为了获得乙烯、丙烯、丁二烯、丁烯等.
解答 解:A、煤液化是把固体煤炭通过化学加工过程,使其转化成为液体燃料、化工原料和产品的先进洁净煤技术,不能获得芳香烃,故A错误;
B、催化重整是在加热、加压和催化剂存在的条件下,使原油蒸馏所得的轻汽油馏分(或石脑油)转变成富含芳烃的高辛烷值汽油(重整汽油),并副产液化石油气和氢气的过程,故B正确;
C、石油裂化的目的是为了提高轻质液体燃料的产量,特别是提高汽油的产量,故C正确;
D、石油裂解的目的是为了获得乙烯、丙烯、丁二烯、丁烯等不饱和烯烃,故D正确;
故选A.
点评 本题考查了石油、煤的综合利用,难度不大,注意煤的直接液化和间接液化的区别、石油裂化、裂解的区别.


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:解答题
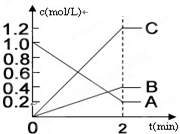 (1)铅蓄电池是常用的化学电源,其电极材料是Pb和PbO2,电解液为稀硫酸.工作时该电池总反应式为PbO2+Pb+2H2SO4═2PbSO4+2H2O,据此判断:
(1)铅蓄电池是常用的化学电源,其电极材料是Pb和PbO2,电解液为稀硫酸.工作时该电池总反应式为PbO2+Pb+2H2SO4═2PbSO4+2H2O,据此判断:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
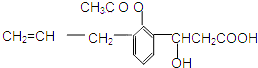
| A. | 可发生的反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和 | |
| B. | 该物质1mol与足量NaOH溶液反应,消耗NaOH的物质的量为2mol | |
| C. | 可与氯化铁溶液发生显色反应 | |
| D. | 该有机物属于芳香烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表中,除第一和第七周期外,第n周期所含非金属元素的种数均为(8-n) | |
| B. | SiCl4、PCl3分子中各原子最外层均达到8电子稳定结构 | |
| C. | 气态氢化物的水溶液都是酸 | |
| D. | ⅠA族和ⅥA族元素形成的原子个数比1:1、电子总数38的化合物,是有共价键的离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与氯气反应 | B. | 次氯酸的分解 | ||
| C. | 乙醇与乙酸的酯化反应 | D. | 甲烷与氧气的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠、过氧化钠、硫酸四氨合铜[Cu(NH3)4]SO4、氢化钠 | |
| B. | 硝酸铵、氢化铵、氢氧化二氨合银[Ag(NH3)2]OH、硫酸铵 | |
| C. | 硫酸、氢氧化钠、氮化钙、氢氧化钡 | |
| D. | 氯化铵、氢氧化钠、双氧水、过氧化钙 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
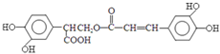
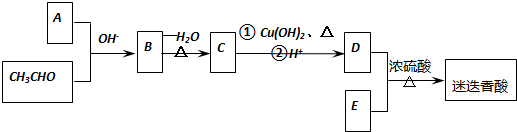
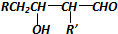 $→_{-H_{2}O}^{△}$
$→_{-H_{2}O}^{△}$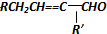
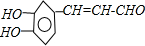 .
.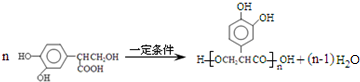 .
.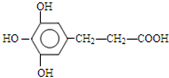 、
、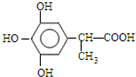 、
、 、
、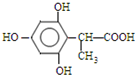 (任一种).
(任一种).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com