
���� A��B��C��D ��Ԫ�����ڱ���ǰ20��Ԫ�أ�ԭ��������������B��C��D ͬ���ڣ�B��C��D������������ˮ����������Ͼ��ܷ�����Ӧ��Ӧ������������ǿ�ǿ��֮��ķ�Ӧ������֪BΪNa��CΪAl��A��Dͬ���壬��AΪO��DΪS����AΪF��DΪCl��E������Ԫ�ؼȲ���ͬ����Ҳ����ͬ���壬����֪EΪCa���ݴ˽��
��� �⣺A��B��C��D ��Ԫ�����ڱ���ǰ20��Ԫ�أ�ԭ��������������B��C��D ͬ���ڣ�B��C��D������������ˮ����������Ͼ��ܷ�����Ӧ��Ӧ������������ǿ�ǿ��֮��ķ�Ӧ������֪BΪNa��CΪAl��A��Dͬ���壬��AΪO��DΪS����AΪF��DΪCl��E������Ԫ�ؼȲ���ͬ����Ҳ����ͬ���壬����֪EΪCa��
��1��A��Dͬ���壬ԭ������A��D���ʷǽ�����A��D���ʶ����⻯���У�D���⻯���ȶ��Խ�����A��B�����Ӻ����������Ϊ10��B������Ϊ Na+���˵��������A���ʰ뾶��С���� Na+���ʴ�Ϊ��D��Na+��
��2��CΪAl��ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ3���������ڱ��е������ڢ�A�壬�ʴ�Ϊ���������ڢ�A�壻
��3��������������֪��EΪ��Ԫ�أ��ʴ�Ϊ���ƣ�
���� ���⿼��ṹ����λ�ù�ϵӦ�ã����ݡ�B��C��D������������ˮ����������Ͼ��ܷ�����Ӧ���С��ƶϣ��ѶȲ���


 ͬ������ϵ�д�
ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
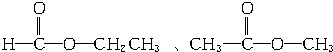 ��
��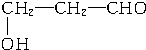 ��
��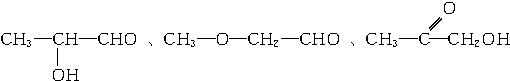 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
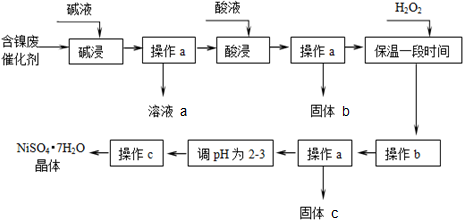
| ������ | ��ʼ���� | ��ȫ���� |
| Al��OH��3 | 3.8 | 5.2 |
| Fe��OH��3 | 2.7 | 3.2 |
| Fe��OH��2 | 7.6 | 9.7 |
| Ni��OH��2 | 7.1 | 9.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ�ﵽƽ��ʱ���ų�����������92.4KJ | |
| B�� | �ﵽƽ�����������ͨ��1mol������ƽ�ⲻ�ƶ� | |
| C�� | �����¶Ⱥ���С�����������ʹ�÷�Ӧ��ƽ�ⳣ������ | |
| D�� | ���ﵽƽ��ʱN2��ת����Ϊ20%����ƽ��ʱ�����ڵ�ѹǿ����ʼʱ��80% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ԫ��A�ĵ��ʲ��ܰѽ���Ԫ��B����������Һ���û�������һ������˵�������ԣ�A��B | |
| B�� | ���ݷ�Ӧ2C+SiO2$\frac{\underline{\;����\;}}{\;}$Si+2CO������˵��C�ķǽ����Ա�Siǿ | |
| C�� | ���ڱ��е�n���ڵ�n�����Ԫ�ؾ�Ϊ���� | |
| D�� | ����Ԫ�����ڱ����Ų����ɣ��ǽ���Ԫ�����Ϊ23�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
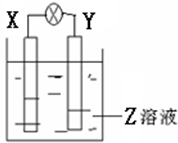 ��ͼ��ʾװ���У��۲쵽������ָ��ƫת��X�����أ�Y�����ᣬ�ɴ��ж��±�������X��Y��Z���ʣ����п��Գ������ǣ�������
��ͼ��ʾװ���У��۲쵽������ָ��ƫת��X�����أ�Y�����ᣬ�ɴ��ж��±�������X��Y��Z���ʣ����п��Գ������ǣ�������| X | Y | Z | |
| A | п | ͭ | ϡ������Һ |
| B | ͭ | �� | ϡ���� |
| C | п | ͭ | ��������Һ |
| D | ̼ | п | ����ͭ��Һ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������Һ�������У�Ӧ������ˮ��ϴ����ϴ��գ�۾� | |
| B�� | ������Ũ��Һմ��Ƥ���ϣ�Ҫ�����ô���ˮ��ϴ��Ȼ��Ϳ��С�մ���Һ | |
| C�� | �ڼ��ȵ�����£��Թ��е�Һ�������Ҫ�����Թ��ݻ���$\frac{3}{4}$ | |
| D�� | ����������Һʱ����������Ͳ�м���һ�������ˮ�����ڽ�������������Ũ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com