
【题目】氮化铝(AlN)是一种新型无机非金属材料。某AlN样品仅含有Al2O3杂质,为测定AlN的含量,设计如下三种实验方案。
已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。
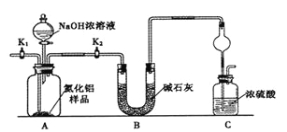
(1)上图C装置中球形干燥管的作用是 。
(2)完成以下实验步骤:组装好实验装置,首先 ,再加入实验药品。接下来的实验操作是 ,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见
【方案2】用右图装置测定m g样品中A1N的纯度(部分夹持装置已略去)。
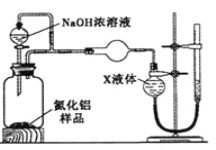
(4)为测定生成气体的体积,量气装置中的X液体可以是 。
a.CCl4 b.H2O
c.NH4Cl溶液 d.苯
(5)若m g样品完全反应,测得生成气体的体积为V mL(已转换为标准状况),则AIN的质量分数是 。
【方案3】按以下步骤测定样品中A1N的纯度:
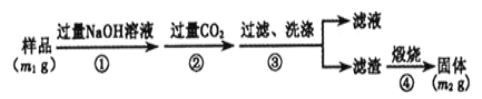
(6)步骤②生成沉淀的离子方程式为 。
【答案】
(1)防止倒吸;
(2)检查装置气密性,关闭K1,打开K2,把装置中残留的氨气全部赶入C装置;
(3)C装置出口处连接一个干燥装置;
(4)ad(5)![]() ×100%;
×100%;
(6)CO2+AlO2-+2H2O=HCO3-+Al(OH)3↓。
【解析】
试题分析:(1)分析装置和仪器作用分析,氨气是与浓硫酸能发生反应的气体,易发生倒吸,图C装置中球形干燥管的作用是防止倒吸的作用,故答案为:防止倒吸;
(2)组装好实验装置,原理可知气体制备需要先检查装置气密性,加入实验药品.接下来的实验操作是关闭K1,打开K2,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体.打开K1,通入氮气一段时间,测定C装置反应前后的质量变化.通入氮气的目的是,反应生成氨气后卫把装置中的气体全部赶入装置C被浓硫酸吸收,准确测定装置C的增重计算,故答案为:检查装置气密性,关闭K1,打开K2,把装置中残留的氨气全部赶入C装置;
(3)装置存在缺陷是空气中的水蒸气和二氧化碳也可以进入装置C,使测定结果偏高,需要连接一个盛碱石灰干燥管,故答案为:C装置出口处连接一个干燥装置;
(4)依据氨气极易溶于水的性质分析,为测定生成气体的体积,量气装置中的X液体可以是;a.CCl4不能溶解氨气,可以用排四氯化碳溶液的方法测定氨气体积,故a正确; b.氨气极易溶于水,不能排水法测定,故b错误;c.氨气极易溶于水,不能用排NH4Cl溶液的方法测定气体体积,故c错误;d.氨气不溶于苯,可以利用排苯溶液,测定氨气的体积,故d正确;故选ad.
(5)若m g样品完全反应,测得生成气体的体积为V mL(已转换为标准状况),
AIN+NaOH+H2O═NaAIO2+NH3↑
41 22.4L
m V×10-3L
m=![]() ,则AlN的质量分数=
,则AlN的质量分数=![]() ×100%=
×100%=![]() ×100%,故答案为:
×100%,故答案为:![]() ×100%;
×100%;
(6)步骤②生成的沉淀是氢氧化铝,是偏铝酸钠溶液中通入过量二氧化碳气体反应生成,反应的离子方程式为:CO2+AlO2-+2H2O=HCO3-+Al(OH)3↓,故答案为:CO2+AlO2-+2H2O=HCO3-+Al(OH)3↓。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】下列反应中,属于加成反应的是( )
A.甲烷与氯气的混合气体在光照条件下反应
B.丙烯和氯气在一定条件下反应生成ClCH2CH===CH2的反应
C.乙烯使酸性高锰酸钾溶液褪色
D.乙烯与HCl气体反应生成一氯乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下面是我们熟悉的物质:
①O2②SO2③CaCl2④HNO3⑤NaOH ⑥NH4Cl
这些物质中,属于共价化合物的是 ___________;属于离子化合物的是___________;只含离子键的是___________。
(2)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
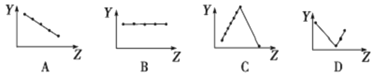
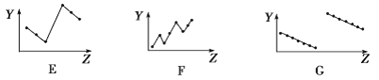
把与下面的元素有关性质相符的曲线的标号填入相应括号中:
①第ⅡA族元素的最外层电子数________________。
②第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径________________。
③第二、三周期主族元素随原子序数递增原子半径的变化____________。
(3)已知某单核粒子的结构示意图为:![]()
①当x-y=10时,该粒子为____________(填“原子”、“阳离子”或“阴离子”)。
②当y=8时,若该微粒的氧化性很弱,得一个电子后变为原子,该微粒的符号是_____________。
(4)已知A、B、C、D是中学化学中常见的四种10电子微粒,
它们之间存在如图中转化关系。
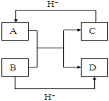
请写出:A的化学式 (写一种);D的化学式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O![]() Fe(OH)2+2Ni(OH)2.下列有关该电池的说法不正确的是( )
Fe(OH)2+2Ni(OH)2.下列有关该电池的说法不正确的是( )
A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe
B.电池放电时,负极反应为Fe-2e-![]() Fe2+
Fe2+
C.电池充电过程中,阴极附近溶液的pH升高
D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-![]() Ni2O3+3H2O
Ni2O3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个容积相同的容器中,一个盛有NH3,另一个盛有N2、H2的混合气体,在同温同压下,两容器内的气体一定具有相同的
A. 原子数 B. 分子数 C. 质量 D. 密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物能使澳的CC4溶液褪色,也能在一定条件下发生水解生成两种有机物,还能发生加聚反应生成高分子化合物,则此有机物中通常含有的基团的组合是
A. 卤素原子、碳碳双键 B. 羟基、羧基 C. 醛基、酯基 D. 碳碳双键、酯基
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式: .若1g水蒸气转化成液态水放热2.5kJ,则氢气的燃烧热为△H= kJ/mol.
(2)近年来已经研制出甲烷(CH4)燃料电池,该电池的电解质溶液为H2SO4溶液,写出该电池负极的电极反应式: .该电池总反应式: .
(3)用惰性电极电解AgNO3溶液,写出该电解反应的化学方程式 ;若在阳极收集到 0.32g O2,中和电解生成的酸需0.4molL﹣1NaOH溶液 mL.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com