
2015年10月5日,中国科学家屠呦呦首次获诺贝尔生理学或医学奖,以表彰她发现了一种药物——青蒿素,它是由菊科植物在低湿条件下提炼出来的一种化合物,是治疗疟疾的特效药,其结构简式如图所示。下列有关青蒿素的说法不正确的是
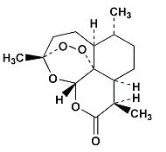
A.青蒿素的分子式为C15H22O5
B.青蒿素不易溶于水,可溶于乙醚
C.青蒿素在一定条件下可发生水解、取代、加成、氧化反应
D.青蒿素分子内的一个过氧基团是对付疟原虫的核心基团
科目:高中化学 来源:2015-2016学年湖南常德石门第一中学高二上期中文化学卷(解析版) 题型:选择题
不属于人体能够消化吸收的营养物质的是
A.糖类、油脂 B.蛋白质、淀粉 C.纤维素 D.水、矿物质
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西柳州铁路第一中学高一上段考化学试卷(解析版) 题型:推断题
A、B、C、D、F五种物质的焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃气体,而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变浑浊。D和A可反应生成C,F和H也可反应生成C和另一种无色无味气体。请回答下列问题:
(1)写出A、B、E的化学式:A_______________;B_______________;E_______________
(2)写出F和H反应的化学方程式 。
(3)按要求写方程式:
① 加热固体D发生反应的化学反应方程式 。
② C与足量盐酸反应的离子方程式 。
③ A溶液与金属铝反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省嘉兴、杭州、宁波五校高三上第一次联考化学试卷(解析版) 题型:选择题
下列依据热化学方程式得出的结论正确的是
A.若2H2(g)+O2(g) =2H2O(g)ΔH=-483.6 kJ·mol-1,则H2的标准燃烧热为-241.8 kJ·mol-1
B.若C(石墨,s) =C(金刚石,s) ΔH>0,则石墨比金刚石稳定
C.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1,则20.0g NaOH固体与稀盐酸完全中和,放出28.7 kJ的热量
D.已知2C(s)+2O2(g) =2CO2(g) ΔH1;2C(s)+O2(g) =2CO(g) ΔH2,则ΔH1>ΔH2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西桂林中学高二上期中考试文化学试卷(解析版) 题型:选择题
下列实验仪器不宜直接用来加热的是( )
A.试管 B.坩埚 C.蒸发皿 D.烧杯
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东深圳高级中学高一上期中考试化学试卷(解析版) 题型:填空题
氯化钠是日常生活的必需品,也是重要的化工原料。粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是粗盐提纯的操作流程。
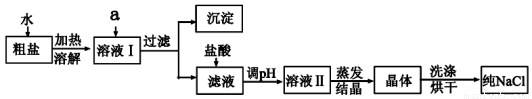
限选试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液。
(1)欲除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:过量的NaOH溶液、_________、________;生 成的沉淀含有的成分为泥沙、________。
成的沉淀含有的成分为泥沙、________。
(2)在滤液中加盐酸发生反应的离子方程式是____________________________________;
(3)对溶液II处理得到晶体时,所必须使用到的玻璃仪器有_________种。
(4)得到的NaCl纯品经测定发现其含有的NaCl与粗盐中NaCl的质量一致,某同学认为此次实验非常成功没有误差,你是否同意他的观点?_______(填“是”或“否”),并给出你的理由_______。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东深圳高级中学高二上期中考试化学试卷(解析版) 题型:选择题
某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如下图所示。据图分析,下列判断不正确的是
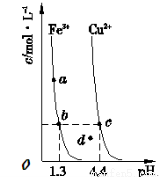
A.Ksp[Fe(OH)3]<Ksp[Cu(OH)2 ]
B.加适量NH4 Cl固体可使溶液由a点变到b点
C.c、d两点代表的溶液中c(H+ )与c(OH-)乘积相等
D.Fe(OH)3 、Cu(OH)2 分别在b、c两点代表的溶液中达到饱和
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东广州执信中学高二上期中文化学试卷(解析版) 题型:?????
下列反应的离子方程式不正确的是
A.氯化钡和稀硫酸反应:Ba2++SO42- = BaSO4↓
B.铁与稀盐酸反应:2Fe + 6H+ = 2Fe3+ + 3H2↑
C.锌与硫酸铜溶液反应:Zn+Cu2+ = Zn2++Cu
D.氢氧化钠和盐酸反应:OH-+ H+ = H2O
查看答案和解析>>
科目:高中化学 来源:2016届安徽省合肥市高三上学期期中考试化学试卷(解析版) 题型:填空题
乙醇是重要的有机化工原料,可由乙烯直接水合法或间接水合法生产。回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H)。再水解生成乙醇。写出相应的反应的化学方程式 。
(2)已知:乙烯气相直接水合反应如下:
C2H4(g)+H2O(g) 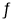 C2H5OH(g) H=-45.5KJ/mol
C2H5OH(g) H=-45.5KJ/mol
下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系(其中n(H2O):n(C2H4)=1:1)
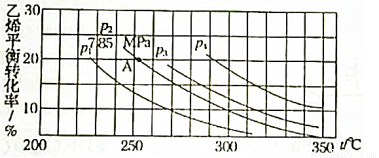
①计算乙烯水合制乙醇反应在图中A点的平衡常数Kp= (Kp表示用平衡分压代替平衡浓度计算出的平衡常数的值,分压=总压×物质的量分数)
②图中压强P1、P2、P3、P4的大小顺序为: ,理由是 。
(3)若某温度下,反应C2H4(g)+H2O(g) 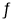 C2H5OH(g)的平衡常数为Kp=0.05MPa-1,体系总压为8.00MPa,各物质的量分数如下表所示。
C2H5OH(g)的平衡常数为Kp=0.05MPa-1,体系总压为8.00MPa,各物质的量分数如下表所示。
物质 | C2H4(g) | H2O(g) | C2H5OH(g) |
物质的量分数 | 0.25 | 0.25 | 0.5 |
则v(正) v(逆)(填“>”“<”“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com